10. 关于 $CO_{2}$ 与 $CO$ 的知识总结错误的是 (
A.构成:一个二氧化碳分子比一个一氧化碳分子多一个氧原子
B.性质:通常情况下,$CO_{2}$ 不支持燃烧;$CO$ 支持燃烧
C.用途:固体 $CO_{2}$ 可作制冷剂
D.危害:$CO_{2}$ 无毒;$CO$ 易与血液中的血红蛋白结合引起中毒
B
)A.构成:一个二氧化碳分子比一个一氧化碳分子多一个氧原子
B.性质:通常情况下,$CO_{2}$ 不支持燃烧;$CO$ 支持燃烧
C.用途:固体 $CO_{2}$ 可作制冷剂
D.危害:$CO_{2}$ 无毒;$CO$ 易与血液中的血红蛋白结合引起中毒
答案:B
解析:
解:A. 构成:一个二氧化碳分子比一个一氧化碳分子多一个氧原子,正确。
B. 性质:通常情况下,CO₂不支持燃烧;CO具有可燃性,而非支持燃烧,错误。
C. 用途:固体CO₂(干冰)可作制冷剂,正确。
D. 危害:CO₂无毒;CO易与血液中的血红蛋白结合引起中毒,正确。
结论:B
B. 性质:通常情况下,CO₂不支持燃烧;CO具有可燃性,而非支持燃烧,错误。
C. 用途:固体CO₂(干冰)可作制冷剂,正确。
D. 危害:CO₂无毒;CO易与血液中的血红蛋白结合引起中毒,正确。
结论:B
11. 已知白磷的着火点是 $40^{\circ}C$,红磷的着火点是 $240^{\circ}C$。进行如图实验,三支试管里面充满氮气,初始温度为 $25^{\circ}C$,升温至 $60^{\circ}C$ 后,用注射器同时向②③试管中迅速注入足量氧气。下列说法错误的是 (
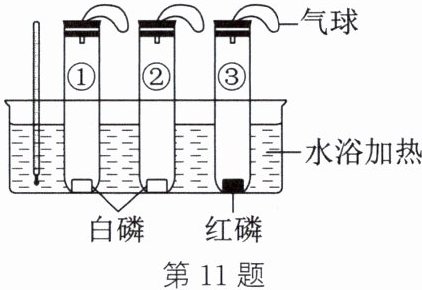
A.只有②中有燃烧现象
B.由①②现象说明可燃物的温度达到着火点也未必能燃烧
C.若继续水浴升温,则③中红磷一定会燃烧
D.该实验能总结出燃烧的条件
C
)
A.只有②中有燃烧现象
B.由①②现象说明可燃物的温度达到着火点也未必能燃烧
C.若继续水浴升温,则③中红磷一定会燃烧
D.该实验能总结出燃烧的条件
答案:C
解析:
燃烧需要同时满足三个条件:可燃物、与氧气(或空气)接触、温度达到可燃物的着火点。
①试管中白磷初始处于氮气环境(无氧气),升温至60°C(达到白磷着火点40°C),但因缺乏氧气,不燃烧;②试管中白磷升温至60°C(达到着火点)后注入氧气(与氧气接触),满足燃烧三条件,会燃烧;③试管中红磷着火点240°C,升温至60°C(未达到着火点),注入氧气后仍不燃烧。
A. 只有②中有燃烧现象,正确;
B. ①中白磷温度达着火点但无氧气不燃烧,②中白磷温度达着火点且有氧气燃烧,说明可燃物温度达到着火点未必能燃烧(需与氧气接触),正确;
C. 若继续水浴升温,未明确升温后的具体温度是否能达到红磷着火点240°C,若升温后温度仍低于240°C,③中红磷不会燃烧,错误;
D. 该实验通过对比①②(验证氧气的必要性)、②③(验证温度达到着火点的必要性),能总结出燃烧的条件,正确。
答案:C
①试管中白磷初始处于氮气环境(无氧气),升温至60°C(达到白磷着火点40°C),但因缺乏氧气,不燃烧;②试管中白磷升温至60°C(达到着火点)后注入氧气(与氧气接触),满足燃烧三条件,会燃烧;③试管中红磷着火点240°C,升温至60°C(未达到着火点),注入氧气后仍不燃烧。
A. 只有②中有燃烧现象,正确;
B. ①中白磷温度达着火点但无氧气不燃烧,②中白磷温度达着火点且有氧气燃烧,说明可燃物温度达到着火点未必能燃烧(需与氧气接触),正确;
C. 若继续水浴升温,未明确升温后的具体温度是否能达到红磷着火点240°C,若升温后温度仍低于240°C,③中红磷不会燃烧,错误;
D. 该实验通过对比①②(验证氧气的必要性)、②③(验证温度达到着火点的必要性),能总结出燃烧的条件,正确。
答案:C
12. A、B、C、D 都是初中化学常见的物质,它们之间的转化关系如图所示(“→”表示物质间的转化关系),已知 A 和 D 均为单质,B 和 C 都是氧化物且组成元素相同,常温下 B、C、D 都是气体,自然界中的绿色植物可实现 $C→D$ 的转化。下列说法不正确的是 (

A.B 是造成“煤气中毒”的主要原因
B.D 的化学性质活泼,能供给呼吸
C.要实现 $A→B$ 只有一种反应途径
D.$A→C$ 可用化学方程式表示为 $C + O_{2}\xlongequal{点燃}CO_{2}$
C
)
A.B 是造成“煤气中毒”的主要原因
B.D 的化学性质活泼,能供给呼吸
C.要实现 $A→B$ 只有一种反应途径
D.$A→C$ 可用化学方程式表示为 $C + O_{2}\xlongequal{点燃}CO_{2}$
答案:C 解析:B 和 C 都是氧化物且组成元素相同,常温下 B、C 都是气体,则 B、C 分别是二氧化碳与一氧化碳中的一种;A 和 D 均为单质,自然界中的绿色植物可实现 $ C \to D $ 的转化,则 A 为碳,D 为氧气,C 为二氧化碳,B 为一氧化碳。由分析可知,B 为一氧化碳,是造成“煤气中毒”的主要原因,A 正确;D 为氧气,其化学性质活泼,能供给呼吸,B 正确;A 为碳,B 为一氧化碳,碳在氧气不足时燃烧能够生成一氧化碳,碳还能与二氧化碳在高温条件下反应生成一氧化碳,C 错误;A 为碳,C 为二氧化碳,则 $ A \to C $ 的反应可以是碳和氧气在点燃的条件下反应生成二氧化碳,反应可用化学方程式表示为 $ C + O_2 \xlongequal{点燃} CO_2 $,D 正确。故本题选 C。
13. 下列框图中的物质均为初中化学常见的物质,其中 A 是天然气的主要成分,C 是黑色固体单质,F 是氧化物,I 是石灰石的主要成分(提示:氧化钙能与水反应生成氢氧化钙)。

(1)写出反应①的化学方程式:
(2)写出反应②的化学方程式:
(3)写出 H 的一种用途:

(1)写出反应①的化学方程式:
$ 2C + O_2 \xlongequal{点燃} 2CO $
。(2)写出反应②的化学方程式:
$ CaO + H_2O = Ca(OH)_2 $
。(3)写出 H 的一种用途:
灭火 (合理答案均可)
。答案:(1) $ 2C + O_2 \xlongequal{点燃} 2CO $ (2) $ CaO + H_2O = Ca(OH)_2 $ (3) 灭火 (合理答案均可)
14. (2024·无锡江阴段考)如图甲是初中化学常用的实验装置,请回答下列问题。

(1)仪器 a 的名称是
(2)实验室制取二氧化碳气体,发生反应的化学方程式为
(3)为了能更加准确地了解二氧化碳溶于水的情况,兴趣小组同学用数字实验测量了反应前后容器内压强的变化,实验装置如图乙所示,装置的气密性良好(图乙中 b 处连接气体压力传感器)。烧瓶内收集满 $CO_{2}$,迅速将注射器内的 $20mL$ 水全部注入烧瓶中,并保持注射器活塞在注射器底部,瓶内压强变化曲线如图丙所示。
① $BC$ 段压强上升的原因是
② $D$ 点压强大于 $B$ 点,说明反应后容器内压强略大于反应前容器内的压强,对此你的解释是

(1)仪器 a 的名称是
水槽
。(2)实验室制取二氧化碳气体,发生反应的化学方程式为
$ CaCO_3 + 2HCl = CaCl_2 + H_2O + CO_2 \uparrow $
,装置 B 和 C 都能用作制取二氧化碳的发生装置,与装置 B 相比,装置 C 的优点是可以随时控制反应的发生和停止
。若用装置 C 作发生装置,关闭止水夹,反应停止后,试管中液面应位于3
(填“1”“2”或“3”)处。若用装置 E 收集二氧化碳,气体应从m
(填“m”或“n”)端进入。(3)为了能更加准确地了解二氧化碳溶于水的情况,兴趣小组同学用数字实验测量了反应前后容器内压强的变化,实验装置如图乙所示,装置的气密性良好(图乙中 b 处连接气体压力传感器)。烧瓶内收集满 $CO_{2}$,迅速将注射器内的 $20mL$ 水全部注入烧瓶中,并保持注射器活塞在注射器底部,瓶内压强变化曲线如图丙所示。
① $BC$ 段压强上升的原因是
水被快速注入烧瓶,造成气体被压缩,压强增大
。② $D$ 点压强大于 $B$ 点,说明反应后容器内压强略大于反应前容器内的压强,对此你的解释是
二氧化碳溶于水的体积小于所加水的体积
。答案:(1) 水槽 (2) $ CaCO_3 + 2HCl = CaCl_2 + H_2O + CO_2 \uparrow $ 可以随时控制反应的发生和停止 3 m (3) ① 水被快速注入烧瓶,造成气体被压缩,压强增大 ② 二氧化碳溶于水的体积小于所加水的体积