1. 如图所示实验中①、④为用紫色石蕊溶液润湿的棉球,②、③为用石蕊溶液染成紫色的干燥棉球。下列能说明${CO2}$密度大于空气且能与水反应的现象是 (

A.①变红,③不变红
B.④比①先变红,②、③不变红
C.①、④变红,③不变红
D.④变红,③不变红
B
)
A.①变红,③不变红
B.④比①先变红,②、③不变红
C.①、④变红,③不变红
D.④变红,③不变红
答案:【解析】:
本题主要考查二氧化碳的性质,包括其密度比空气大以及能与水反应生成碳酸使紫色石蕊变红的特性。
①、④为用紫色石蕊溶液润湿的棉球,②、③为用石蕊溶液染成紫色的干燥棉球。二氧化碳不能使石蕊变色,二氧化碳与水反应生成的碳酸能使石蕊变色。
A选项:①变红,③不变红,只能说明二氧化碳与水反应生成了能使石蕊变红的物质,但不能体现二氧化碳密度大于空气,所以该选项错误。
B选项:④比①先变红,说明二氧化碳密度比空气大,先在下面聚集;②、③不变红,说明干燥的二氧化碳不能使石蕊变色,即二氧化碳与水反应生成了能使石蕊变红的物质,该选项能全面说明二氧化碳密度大于空气且能与水反应,所以该选项正确。
C选项:①、④变红,③不变红,能说明二氧化碳与水反应生成了能使石蕊变红的物质,但无法体现二氧化碳密度大于空气,所以该选项错误。
D选项:④变红,③不变红,只能说明二氧化碳与水反应生成了能使石蕊变红的物质,不能体现二氧化碳密度大于空气,所以该选项错误。
【答案】:B
本题主要考查二氧化碳的性质,包括其密度比空气大以及能与水反应生成碳酸使紫色石蕊变红的特性。
①、④为用紫色石蕊溶液润湿的棉球,②、③为用石蕊溶液染成紫色的干燥棉球。二氧化碳不能使石蕊变色,二氧化碳与水反应生成的碳酸能使石蕊变色。
A选项:①变红,③不变红,只能说明二氧化碳与水反应生成了能使石蕊变红的物质,但不能体现二氧化碳密度大于空气,所以该选项错误。
B选项:④比①先变红,说明二氧化碳密度比空气大,先在下面聚集;②、③不变红,说明干燥的二氧化碳不能使石蕊变色,即二氧化碳与水反应生成了能使石蕊变红的物质,该选项能全面说明二氧化碳密度大于空气且能与水反应,所以该选项正确。
C选项:①、④变红,③不变红,能说明二氧化碳与水反应生成了能使石蕊变红的物质,但无法体现二氧化碳密度大于空气,所以该选项错误。
D选项:④变红,③不变红,只能说明二氧化碳与水反应生成了能使石蕊变红的物质,不能体现二氧化碳密度大于空气,所以该选项错误。
【答案】:B
2. 把干燥的紫色石蕊试纸放在${CO2}$气体中,石蕊试纸不变色。将${CO2}$气体通入滴有石蕊指示剂的水中,溶液变红色。再将该溶液敞口加热一段时间,发现溶液的红色褪去,冷却到原温度后,再次通入${CO2}$,溶液又变红色。上述实验现象不能说明的是 (
A.${CO2}$能和水发生化学反应
B.${CO2}$的水溶液具有酸性
C.加热能使${CO2}$水溶液的酸性减弱
D.${CO2}$具有酸性
D
)A.${CO2}$能和水发生化学反应
B.${CO2}$的水溶液具有酸性
C.加热能使${CO2}$水溶液的酸性减弱
D.${CO2}$具有酸性
答案:【解析】:
A选项:实验中,将$CO_2$气体通入滴有石蕊指示剂的水中,溶液变红色,这说明$CO_2$能和水发生化学反应生成了酸,使石蕊变红。故A选项正确。
B选项:由于溶液变红色,说明$CO_2$的水溶液具有酸性,因为酸性物质能使石蕊变红。故B选项正确。
C选项:实验中,将溶液敞口加热一段时间后,红色褪去,说明加热使$CO_2$水溶液的酸性减弱,因为加热可能使$CO_2$的溶解度减小,或者使碳酸分解,从而降低了溶液的酸性。故C选项正确。
D选项:实验中并没有直接证明$CO_2$具有酸性,而是证明了$CO_2$能和水反应生成酸。$CO_2$本身并不具有酸性,而是其水溶液具有酸性。故D选项错误。
【答案】:D
A选项:实验中,将$CO_2$气体通入滴有石蕊指示剂的水中,溶液变红色,这说明$CO_2$能和水发生化学反应生成了酸,使石蕊变红。故A选项正确。
B选项:由于溶液变红色,说明$CO_2$的水溶液具有酸性,因为酸性物质能使石蕊变红。故B选项正确。
C选项:实验中,将溶液敞口加热一段时间后,红色褪去,说明加热使$CO_2$水溶液的酸性减弱,因为加热可能使$CO_2$的溶解度减小,或者使碳酸分解,从而降低了溶液的酸性。故C选项正确。
D选项:实验中并没有直接证明$CO_2$具有酸性,而是证明了$CO_2$能和水反应生成酸。$CO_2$本身并不具有酸性,而是其水溶液具有酸性。故D选项错误。
【答案】:D
3. 如图是初中化学常用的实验装置,请回答下列问题。

A B C D E
(1)仪器a的名称是______
(2)实验室制取二氧化碳气体,发生反应的化学方程式为______
(3)为了能更加准确地了解二氧化碳溶于水的情况,兴趣小组同学用数字实验测量了反应前后容器内压强的变化。实验装置如图所示,装置的气密性良好(图中a处连接气体压力传感器),烧瓶内收集满${CO2}$,注射器内装有20 mL液体。迅速将注射器内液体全部注入烧瓶中,关闭活塞,瓶内压强变化曲线如图所示。
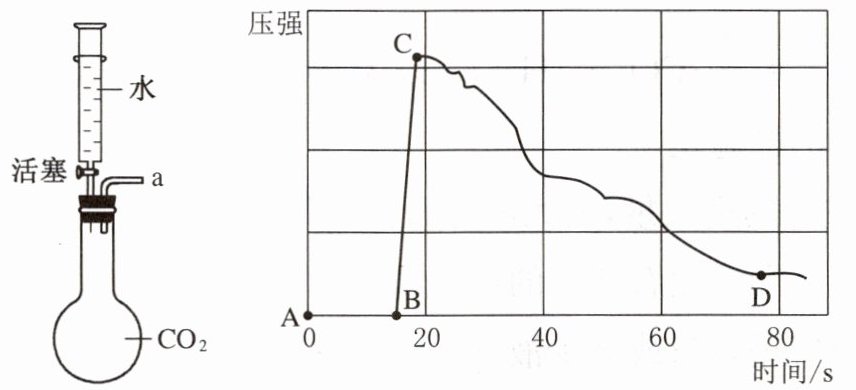
① BC段压强上升的原因是______
② D点压强大于B点,说明反应后容器内压强略大于反应前容器内的压强,对此你的解释是______

A B C D E
(1)仪器a的名称是______
水槽
。(2)实验室制取二氧化碳气体,发生反应的化学方程式为______
CaCO₃+2HCl=CaCl₂+H₂O+CO₂↑
,装置B和C都能用作制取二氧化碳的发生装置,与装置B相比,装置C的优点是______可以控制反应的发生和停止
。若用装置C作发生装置,关闭弹簧夹,反应停止后,液面应位于______2
(填“1”“2”或“3”)处。若用装置D收集二氧化碳,气体应从______m
(填“m”或“n”)端进入。(3)为了能更加准确地了解二氧化碳溶于水的情况,兴趣小组同学用数字实验测量了反应前后容器内压强的变化。实验装置如图所示,装置的气密性良好(图中a处连接气体压力传感器),烧瓶内收集满${CO2}$,注射器内装有20 mL液体。迅速将注射器内液体全部注入烧瓶中,关闭活塞,瓶内压强变化曲线如图所示。

① BC段压强上升的原因是______
注射器内液体迅速注入烧瓶,使瓶内气体体积减小,压强增大
。② D点压强大于B点,说明反应后容器内压强略大于反应前容器内的压强,对此你的解释是______
二氧化碳溶于水的体积小于注入水的体积,导致瓶内气体总体积减小的程度小于液体占据的体积,所以压强略大于反应前
。答案:(1)水槽
(2)$CaCO_{3}+2HCl=CaCl_{2}+H_{2}O+CO_{2}\uparrow $;可以控制反应的发生和停止;2;m
(3)①注射器内液体迅速注入烧瓶,使瓶内气体体积减小,压强增大
②二氧化碳溶于水的体积小于注入水的体积,导致瓶内气体总体积减小的程度小于液体占据的体积,所以压强略大于反应前
(2)$CaCO_{3}+2HCl=CaCl_{2}+H_{2}O+CO_{2}\uparrow $;可以控制反应的发生和停止;2;m
(3)①注射器内液体迅速注入烧瓶,使瓶内气体体积减小,压强增大
②二氧化碳溶于水的体积小于注入水的体积,导致瓶内气体总体积减小的程度小于液体占据的体积,所以压强略大于反应前