14. 下列除杂方法中,错误的是(

D
)
答案:14.D
解析:
解:A. 氧气通过灼热的铜网时与铜反应生成氧化铜,氮气不与铜反应,能除去杂质且没有引入新的杂质,方法正确。
B. 稀硫酸与适量氯化钡溶液反应生成硫酸钡沉淀和盐酸,过滤后可除去杂质,方法正确。
C. 碳酸钠溶液与适量稀硫酸反应生成硫酸钠、水和二氧化碳,能除去杂质且没有引入新的杂质,方法正确。
D. 二氧化碳不支持燃烧,二氧化碳中少量的一氧化碳不能被点燃,且通入氧气会引入新的杂质,方法错误。
结论:错误的是D。
B. 稀硫酸与适量氯化钡溶液反应生成硫酸钡沉淀和盐酸,过滤后可除去杂质,方法正确。
C. 碳酸钠溶液与适量稀硫酸反应生成硫酸钠、水和二氧化碳,能除去杂质且没有引入新的杂质,方法正确。
D. 二氧化碳不支持燃烧,二氧化碳中少量的一氧化碳不能被点燃,且通入氧气会引入新的杂质,方法错误。
结论:错误的是D。
15. 某工厂要用赤铁矿石(主要成分是氧化铁,假设杂质不含铁元素)来炼制生铁。若要炼制含铁96%的生铁63 t,理论上需要含杂质20%的赤铁矿石的质量是(
A.120 t
B.108 t
C.96 t
D.84 t
B
)A.120 t
B.108 t
C.96 t
D.84 t
答案:15.B
解析:
设理论上需要含杂质20%的赤铁矿石的质量为$x$。
纯铁的质量为:$63\ \mathrm{t} × 96\% = 60.48\ \mathrm{t}$
赤铁矿石中氧化铁的质量为:$x × (1 - 20\%) = 0.8x$
氧化铁($\mathrm{Fe}_2\mathrm{O}_3$)中铁元素的质量分数为:$\frac{2 × 56}{2 × 56 + 3 × 16} × 100\% = \frac{112}{160} × 100\% = 70\%$
根据铁元素质量守恒可得:$0.8x × 70\% = 60.48\ \mathrm{t}$
解得:$x = 108\ \mathrm{t}$
B
纯铁的质量为:$63\ \mathrm{t} × 96\% = 60.48\ \mathrm{t}$
赤铁矿石中氧化铁的质量为:$x × (1 - 20\%) = 0.8x$
氧化铁($\mathrm{Fe}_2\mathrm{O}_3$)中铁元素的质量分数为:$\frac{2 × 56}{2 × 56 + 3 × 16} × 100\% = \frac{112}{160} × 100\% = 70\%$
根据铁元素质量守恒可得:$0.8x × 70\% = 60.48\ \mathrm{t}$
解得:$x = 108\ \mathrm{t}$
B
16. 化学就在我们身边。请从下列物质中选择相应的序号填空:
①石墨 ②活性炭 ③钛合金 ④生石灰 ⑤酒精
(1)实验室常用的燃料是
(2)能用于吸附冰箱异味的是
(3)可用于制铅笔芯的是
(4)常用作食品干燥剂的是
(5)可用于制造人造骨的是
①石墨 ②活性炭 ③钛合金 ④生石灰 ⑤酒精
(1)实验室常用的燃料是
⑤
;(2)能用于吸附冰箱异味的是
②
;(3)可用于制铅笔芯的是
①
;(4)常用作食品干燥剂的是
④
;(5)可用于制造人造骨的是
③
。答案:16.(1)⑤ (2)② (3)① (4)④ (5)③
17. 碳元素形成的物质的种类是最多的,故对碳及其化合物的研究是很有价值的。
(1)碳原子的结构示意图为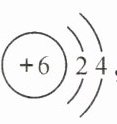 ,碳原子的最外层电子数为
,碳原子的最外层电子数为
(2)酒精是一种含碳元素的化合物,将100 mL酒精和100 mL水混合时,所得液体的体积小于200 mL,原因是
(3)下图是某化学反应前后的微观模拟图,请根据图示回答下列问题。
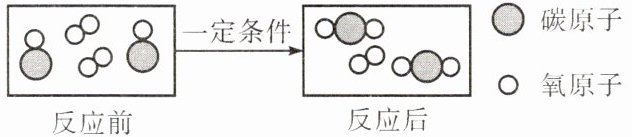
①标出生成物中碳元素的化合价
②写出图示反应的化学方程式:
(4)CO₂在人类生活、生产中具有重要的作用。若要除去CO₂中混有的少量的CO,你的方法是
(1)碳原子的结构示意图为
 ,碳原子的最外层电子数为
,碳原子的最外层电子数为4
。写出一种你知道的碳的单质的名称:金刚石
。(2)酒精是一种含碳元素的化合物,将100 mL酒精和100 mL水混合时,所得液体的体积小于200 mL,原因是
分子之间有间隙
。(3)下图是某化学反应前后的微观模拟图,请根据图示回答下列问题。

①标出生成物中碳元素的化合价
$\mathrm{CO_2^{+4}}$
;②写出图示反应的化学方程式:
$\mathrm{2CO+O_2 \xlongequal{一定条件} 2CO_2}$
。(4)CO₂在人类生活、生产中具有重要的作用。若要除去CO₂中混有的少量的CO,你的方法是
$\mathrm{CO+CuO \xlongequal{加热} Cu+CO_2}$
(用化学方程式表示)。答案:17.(1)4 金刚石 (2)分子之间有间隙 (3)①$\mathrm{CO_2^{+4}}$ ②$\mathrm{2CO+O_2 \xlongequal{一定条件} 2CO_2}$ (4)$\mathrm{CO+CuO \xlongequal{加热} Cu+CO_2}$
18. 溶液在生产、生活中起着十分重要的作用。请回答下列问题。
(1)可以作为溶质的是(
A. 只有固体
B. 只有液体
C. 只有气体
D. 气体、液体、固体都可以
(2)配制100 g质量分数为16%的氯化钠溶液,所需氯化钠的质量为
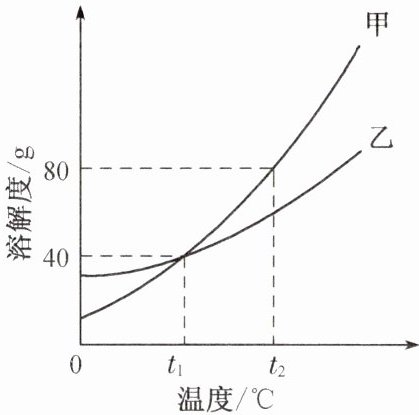
(3)甲、乙两种不含结晶水的固体物质的溶解度曲线如右图所示。t₁℃时,甲物质的溶解度是
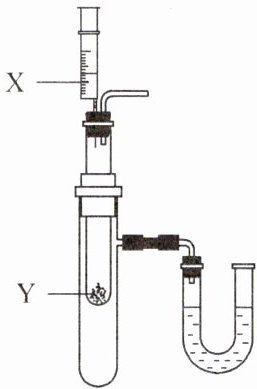
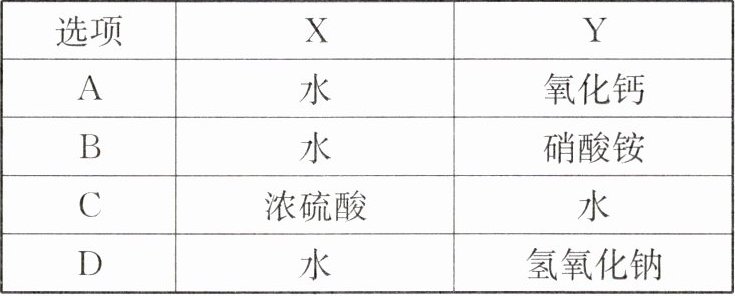
(4)按右图所示装置,将液体X注入装有固体Y的试管中,会导致U形管中右端液面升高,则可能的组合是
(1)可以作为溶质的是(
D
)A. 只有固体
B. 只有液体
C. 只有气体
D. 气体、液体、固体都可以
(2)配制100 g质量分数为16%的氯化钠溶液,所需氯化钠的质量为
16g
,水的体积为84
mL(水的密度近似看作1 g/cm³)。(3)甲、乙两种不含结晶水的固体物质的溶解度曲线如右图所示。t₁℃时,甲物质的溶解度是
40g
。t₂℃时,若从甲和乙两种物质的饱和溶液中析出等质量的固体,须蒸发掉较多水的是乙
(填“甲”或“乙”)物质的饱和溶液。
(4)按右图所示装置,将液体X注入装有固体Y的试管中,会导致U形管中右端液面升高,则可能的组合是
AD
。

答案:18.(1)D (2)16g 84 (3)40g 乙 (4)AD