问题 2. 在溶液中如何确定溶质与溶剂?
要点
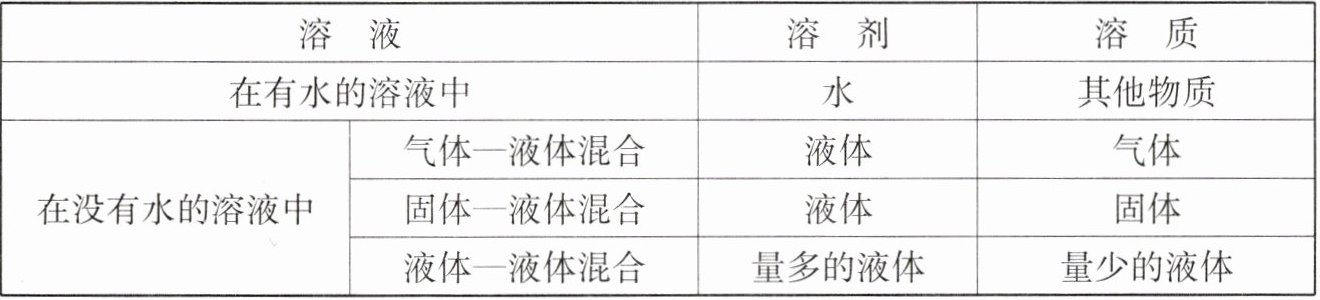
应用
把少量的白磷溶于二硫化碳中制得溶液,其中
要点

应用
把少量的白磷溶于二硫化碳中制得溶液,其中
白磷
是溶质,二硫化碳
是溶剂,这种溶液叫作白磷
的二硫化碳
溶液。答案:问题2. 应用:白磷 二硫化碳 白磷 二硫化碳
解析:
白磷;二硫化碳;白磷;二硫化碳
1. 下列有关溶液的说法正确的是(
A.溶液是混合物
B.溶液一定是无色的
C.均一、稳定的液体一定是溶液
D.植物油和水可以形成溶液
A
)A.溶液是混合物
B.溶液一定是无色的
C.均一、稳定的液体一定是溶液
D.植物油和水可以形成溶液
答案:1. A
2. 下列说法错误的是(
A.溶液是均一、稳定的混合物
B.用于消毒的碘酒是碘的水溶液
C.地球上可供人类直接利用的淡水资源储量很少,我们要节约用水
D.天然淡水经沉降、过滤和灭菌等过程,可以变为生活用的自来水
B
)A.溶液是均一、稳定的混合物
B.用于消毒的碘酒是碘的水溶液
C.地球上可供人类直接利用的淡水资源储量很少,我们要节约用水
D.天然淡水经沉降、过滤和灭菌等过程,可以变为生活用的自来水
答案:2. B
3. 可以作为溶质的是(
A.只有固体
B.只有液体
C.只有气体
D.气体、液体、固体都可以
D
)A.只有固体
B.只有液体
C.只有气体
D.气体、液体、固体都可以
答案:3. D
4. 化学让我们鉴赏了溶液的颜色美。下列物质溶于水后能得到无色溶液的是(
A.CuSO₄
B.MgCl₂
C.KMnO₄
D.FeCl₂
B
)A.CuSO₄
B.MgCl₂
C.KMnO₄
D.FeCl₂
答案:4. B
5. 工业上很多化学反应选择在溶液中进行的主要原因是(
A.反应速率快
B.易于操作
C.不需加热
D.设备简单
A
)A.反应速率快
B.易于操作
C.不需加热
D.设备简单
答案:5. A
6. 在 50 g 稀硫酸中投入 5 g 铁(全部溶解),反应停止后,所得溶液质量是(
A.55 g
B.大于 55 g
C.小于 55 g
D.无法确定
C
)A.55 g
B.大于 55 g
C.小于 55 g
D.无法确定
答案:6. C
解析:
铁与稀硫酸反应的化学方程式为:${Fe + H_2SO_4 = FeSO_4 + H_2↑}$。
参加反应的铁的质量为$5\ \mathrm{g}$,设生成氢气的质量为$x$。
$\begin{aligned}56:2&=5\ \mathrm{g}:x\\56x&=2×5\ \mathrm{g}\\x&=\frac{10}{56}\ \mathrm{g}\approx0.18\ \mathrm{g}\end{aligned}$
反应前溶液质量为$50\ \mathrm{g}$,加入铁的质量为$5\ \mathrm{g}$,生成氢气逸出,逸出氢气质量约$0.18\ \mathrm{g}$。
所得溶液质量为$50\ \mathrm{g}+5\ \mathrm{g}-0.18\ \mathrm{g}=54.82\ \mathrm{g}$,小于$55\ \mathrm{g}$。
C
参加反应的铁的质量为$5\ \mathrm{g}$,设生成氢气的质量为$x$。
$\begin{aligned}56:2&=5\ \mathrm{g}:x\\56x&=2×5\ \mathrm{g}\\x&=\frac{10}{56}\ \mathrm{g}\approx0.18\ \mathrm{g}\end{aligned}$
反应前溶液质量为$50\ \mathrm{g}$,加入铁的质量为$5\ \mathrm{g}$,生成氢气逸出,逸出氢气质量约$0.18\ \mathrm{g}$。
所得溶液质量为$50\ \mathrm{g}+5\ \mathrm{g}-0.18\ \mathrm{g}=54.82\ \mathrm{g}$,小于$55\ \mathrm{g}$。
C
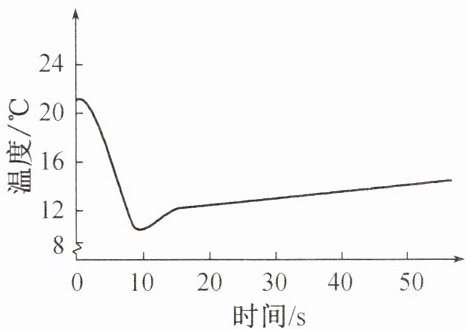
7. 取某固体物质 5 g 加入 20 mL 水中,测得溶液的温度随时间变化的曲线如图所示。该固体物质可能是(
A.NaCl
B.NaOH
C.NH₄NO₃
D.CaCO₃
C
)A.NaCl
B.NaOH

C.NH₄NO₃
D.CaCO₃
答案:7. C
解析:
由图可知,该固体物质溶于水后溶液温度降低。
A. NaCl溶于水温度基本不变,不符合。
B. NaOH溶于水放热,溶液温度升高,不符合。
C. NH₄NO₃溶于水吸热,溶液温度降低,符合。
D. CaCO₃难溶于水,温度无明显变化,不符合。
答案:C
A. NaCl溶于水温度基本不变,不符合。
B. NaOH溶于水放热,溶液温度升高,不符合。
C. NH₄NO₃溶于水吸热,溶液温度降低,符合。
D. CaCO₃难溶于水,温度无明显变化,不符合。
答案:C