7. 小明同学用如图所示装置进行实验。甲瓶中充满二氧化碳气体,注射器中装有氢氧化钠浓溶液,乙中盛有足量稀盐酸。小明先关闭止水夹,然后将氢氧化钠浓溶液全部注入甲瓶,一段时间后再打开止水夹。
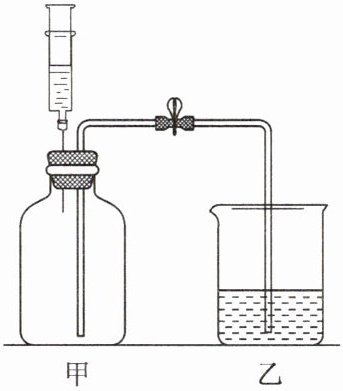
(1)注入氢氧化钠浓溶液后,甲中发生反应的化学方程式为_______。
(2)打开止水夹,可观察到的现象有_______、_______。

(1)注入氢氧化钠浓溶液后,甲中发生反应的化学方程式为_______。
(2)打开止水夹,可观察到的现象有_______、_______。
答案:$7.(1)2\mathrm{NaOH} + \mathrm{CO}_2 =\mathrm{Na}_2\mathrm{CO}_3 + \mathrm{H}_2\mathrm{O} $
(2)乙中液体倒吸入甲中 甲中产生气泡
(2)乙中液体倒吸入甲中 甲中产生气泡
8. 工业烟气脱硫就是将烟气中含有的二氧化硫除去。一种采用“双碱法”脱硫的工业流程示意图如下:
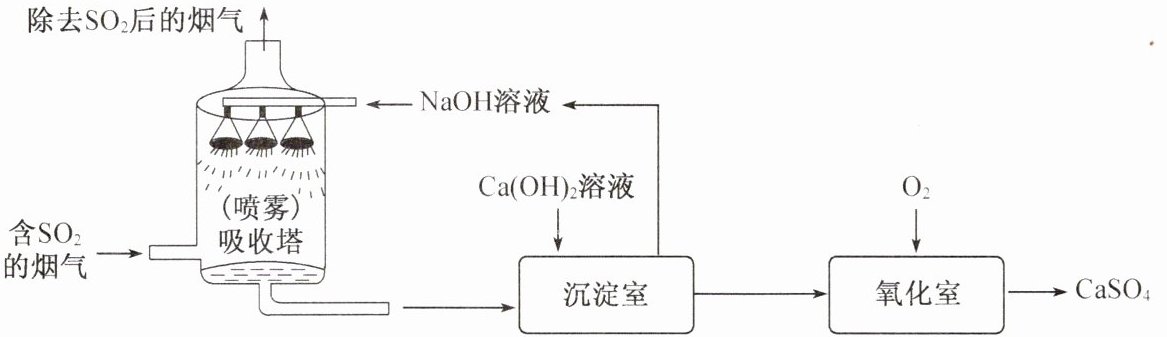
(1)吸收塔中,用${NaOH}$溶液吸收${SO_{2}}$,生成
(2)沉淀室中,发生反应的化学方程式为
(3)氧化室中,化学反应的基本类型是
(4)上述流程中,可以循环利用的物质是

(1)吸收塔中,用${NaOH}$溶液吸收${SO_{2}}$,生成
$\mathrm{Na}_2\mathrm{SO}_3$
和${H_{2}O}$。${NaOH}$溶液喷成雾状能充分吸收${SO_{2}}$的原因是增大接触面积
。(2)沉淀室中,发生反应的化学方程式为
$\mathrm{Na}_2\mathrm{SO}_3 + \mathrm{Ca(OH)}_2 \longrightarrow \mathrm{CaSO}_3 \downarrow + 2\mathrm{NaOH}$
。(3)氧化室中,化学反应的基本类型是
化合
反应。(4)上述流程中,可以循环利用的物质是
$\mathrm{NaOH}$
,有利于节约成本。答案:$8.(1)\mathrm{Na}_2\mathrm{SO}_3 $增大接触面积
$(2)\mathrm{Na}_2\mathrm{SO}_3 + \mathrm{Ca(OH)}_2 \longrightarrow \mathrm{CaSO}_3 \downarrow + 2\mathrm{NaOH} $
(3)化合$ (4)\mathrm{NaOH}$
$(2)\mathrm{Na}_2\mathrm{SO}_3 + \mathrm{Ca(OH)}_2 \longrightarrow \mathrm{CaSO}_3 \downarrow + 2\mathrm{NaOH} $
(3)化合$ (4)\mathrm{NaOH}$