1. 汽车安全气囊系统如图所示,其中气体发生器内产气药剂的信息如资料卡片所示。下列说法错误的是(

A.NaHCO₃ 俗称小苏打
B.Fe₂O₃ 属于氧化物
C.KClO₄ 中钾离子的符号为 K⁺
D.NaN₃ 由三种元素组成
D
)
A.NaHCO₃ 俗称小苏打
B.Fe₂O₃ 属于氧化物
C.KClO₄ 中钾离子的符号为 K⁺
D.NaN₃ 由三种元素组成
答案:1.D
解析:
A. ${NaHCO3}$俗称小苏打,正确。
B. ${Fe2O3}$由两种元素组成且其中一种是氧元素,属于氧化物,正确。
C. ${KClO4}$中钾离子的符号为${K+}$,正确。
D. ${NaN3}$由钠、氮两种元素组成,错误。
答案:D
B. ${Fe2O3}$由两种元素组成且其中一种是氧元素,属于氧化物,正确。
C. ${KClO4}$中钾离子的符号为${K+}$,正确。
D. ${NaN3}$由钠、氮两种元素组成,错误。
答案:D
2. 某同学总结了食盐、纯碱、小苏打和碳酸钙的用途,其中错误的一项是(
A.食盐可用作调味品
B.纯碱可治理盐碱地
C.碳酸钙可作补钙剂
D.小苏打可治疗胃酸过多
B
)A.食盐可用作调味品
B.纯碱可治理盐碱地
C.碳酸钙可作补钙剂
D.小苏打可治疗胃酸过多
答案:2.B
3. 下列是与人类的生产、生活密切相关的物质:
A. 碳酸氢钠
B. 稀盐酸
C. 熟石灰
D. 食盐
E. 木炭
选择相应物质的字母填空:
(1)
(2)
(3)
(4)
(5)
A. 碳酸氢钠
B. 稀盐酸
C. 熟石灰
D. 食盐
E. 木炭
选择相应物质的字母填空:
(1)
E
可用作冰箱除味剂;(2)
B
可用作工业上除铁锈;(3)
A
可用作治疗胃酸过多;(4)
C
可用作农业上改良酸性土壤;(5)
D
是日常生活中一种重要的调味品。答案:3.(1)E (2)B (3)A (4)C (5)D
4. 下列物质的名称、俗名、化学式、类别完全一致的一组是(

C
)
答案:4.C
5. 某化学兴趣小组的同学对酸、碱和盐的性质进行探究,请你参与。
[查阅资料] CO₂ + Na₂CO₃ + H₂O = 2NaHCO₃
20℃时,部分物质的溶解度如下表所示。
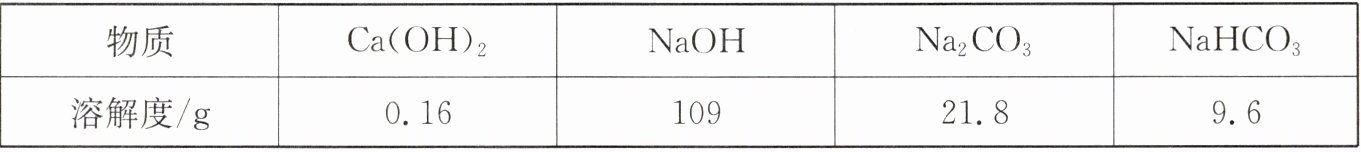
探究一:探究氢氧化钙的性质。
20℃时,在盛有 5g Ca(OH)₂ 固体的 A 烧杯中加入 40mL 水,用玻璃棒搅拌,静置,取上层部分清液于 B 烧杯中。
(1)向 A 烧杯中滴加几滴酚酞溶液,观察到的现象是
(2)向 B 烧杯中通入 CO₂,观察到澄清石灰水变浑浊。
(3)由上述实验可知氢氧化钙的性质为
[实验拓展]
(4)向上述(1)反应后的 A 烧杯中滴加碳酸钠溶液,测得其 pH 随反应时间的变化如图甲所示。AB 段的实验现象是
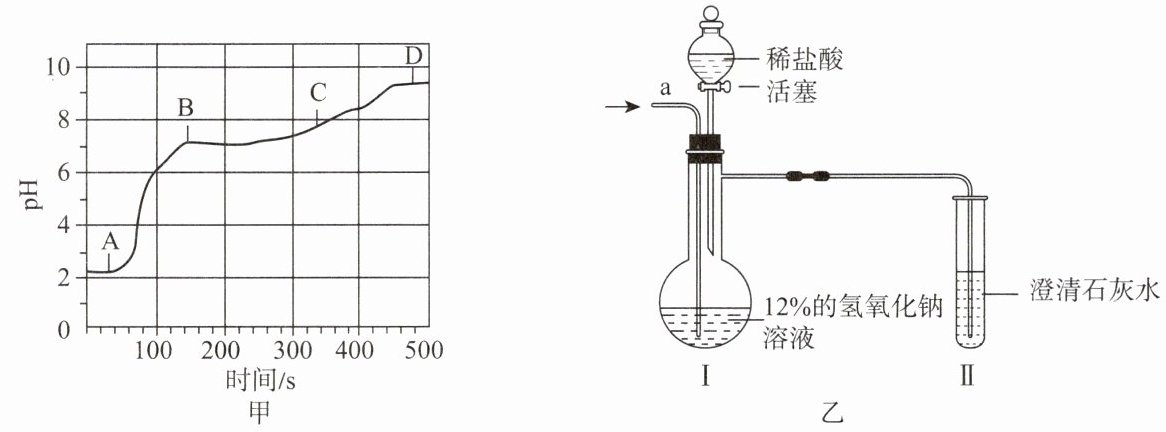
探究二:二氧化碳通入一定溶质质量分数的氢氧化钠溶液中溶质成分的探究。
[设计和实验] 20℃时,甲、乙两组同学设计如图乙所示装置分别进行实验。
(1)甲组:从 a 端缓慢通入 CO₂,一段时间后Ⅱ中溶液变浑浊,停止通 CO₂,Ⅰ中溶质为 X。打开活塞,滴加足量稀盐酸。
解释与结论:经分析 X 是 NaHCO₃。实验过程中,Ⅰ中产生的现象是
(2)乙组:从 a 端缓慢通入 CO₂,一段时间后Ⅱ中无明显现象,停止通 CO₂,Ⅰ中溶质为 Y。打开活塞,滴加足量稀盐酸,Ⅱ 中变浑浊。
解释与结论:乙组同学认为 Y 只有 Na₂CO₃。你认为该结论是否合理?
[查阅资料] CO₂ + Na₂CO₃ + H₂O = 2NaHCO₃
20℃时,部分物质的溶解度如下表所示。

探究一:探究氢氧化钙的性质。
20℃时,在盛有 5g Ca(OH)₂ 固体的 A 烧杯中加入 40mL 水,用玻璃棒搅拌,静置,取上层部分清液于 B 烧杯中。
(1)向 A 烧杯中滴加几滴酚酞溶液,观察到的现象是
溶液由无色变为红色
,再加入过量稀盐酸,反应的化学方程式为Ca(OH)₂+2HCl=CaCl₂+2H₂O
。(2)向 B 烧杯中通入 CO₂,观察到澄清石灰水变浑浊。
(3)由上述实验可知氢氧化钙的性质为
固体;微溶于水,能与指示剂作用;能与某些非金属氧化物反应生成盐和水;能与酸反应生成盐和水
。[实验拓展]
(4)向上述(1)反应后的 A 烧杯中滴加碳酸钠溶液,测得其 pH 随反应时间的变化如图甲所示。AB 段的实验现象是
产生大量气泡
,BC 段发生反应的化学方程式为CaCl₂+Na₂CO₃=CaCO₃↓+2NaCl
。
探究二:二氧化碳通入一定溶质质量分数的氢氧化钠溶液中溶质成分的探究。
[设计和实验] 20℃时,甲、乙两组同学设计如图乙所示装置分别进行实验。
(1)甲组:从 a 端缓慢通入 CO₂,一段时间后Ⅱ中溶液变浑浊,停止通 CO₂,Ⅰ中溶质为 X。打开活塞,滴加足量稀盐酸。
解释与结论:经分析 X 是 NaHCO₃。实验过程中,Ⅰ中产生的现象是
无色溶液中逐渐有固体析出(变浑浊),滴盐酸后有气泡产生,固体逐渐溶解(消失)
。(2)乙组:从 a 端缓慢通入 CO₂,一段时间后Ⅱ中无明显现象,停止通 CO₂,Ⅰ中溶质为 Y。打开活塞,滴加足量稀盐酸,Ⅱ 中变浑浊。
解释与结论:乙组同学认为 Y 只有 Na₂CO₃。你认为该结论是否合理?
不合理
。结合分析 Y 的成分说明理由:根据通入的CO₂的量的不同情况判断,Y的溶质成分可能还有NaOH和Na₂CO₃,Na₂CO₃和NaHCO₃,NaHCO₃这三种情况。三种情况均能与稀盐酸反应产生气体且使澄清石灰水变浑浊
。Ⅰ中一定发生反应的化学方程式为2NaOH+CO₂=Na₂CO₃+H₂O
。答案:5.探究一:(1)溶液由无色变为红色 (2)Ca(OH)₂+2HCl=CaCl₂+2H₂O (3)固体;微溶于水,能与指示剂作用;能与某些非金属氧化物反应生成盐和水;能与酸反应生成盐和水 (4)产生大量气泡 CaCl₂+Na₂CO₃=CaCO₃↓+2NaCl
探究二:(1)无色溶液中逐渐有固体析出(变浑浊),滴盐酸后有气泡产生,固体逐渐溶解(消失) (2)不合理 根据通入的CO₂的量的不同情况判断,Y的溶质成分可能还有NaOH和Na₂CO₃,Na₂CO₃和NaHCO₃,NaHCO₃这三种情况。三种情况均能与稀盐酸反应产生气体且使澄清石灰水变浑浊 2NaOH+CO₂=Na₂CO₃+H₂O
探究二:(1)无色溶液中逐渐有固体析出(变浑浊),滴盐酸后有气泡产生,固体逐渐溶解(消失) (2)不合理 根据通入的CO₂的量的不同情况判断,Y的溶质成分可能还有NaOH和Na₂CO₃,Na₂CO₃和NaHCO₃,NaHCO₃这三种情况。三种情况均能与稀盐酸反应产生气体且使澄清石灰水变浑浊 2NaOH+CO₂=Na₂CO₃+H₂O