1. 复分解反应:两种化合物相互交换成分,生成
注意:复分解反应中,各元素的化合价
另外两种化合物的化学反应
。注意:复分解反应中,各元素的化合价
不变
(填“变”或“不变”)。答案:1.另外两种化合物的化学反应 不变
2. 氢氧化钠溶液中的微观粒子有
$\mathrm{Na}^+$、$\mathrm{OH}^-$、$\mathrm{H}_2\mathrm{O}$
,氢氧化钙溶液中的微观粒子有$\mathrm{Ca}^{2+}$、$\mathrm{OH}^-$、$\mathrm{H}_2\mathrm{O}$
,这两种碱溶液具有相似的化学性质是因为它们的溶液中都含有$\mathrm{OH}^-$
(填离子符号)。答案:2.$\mathrm{Na}^+$、$\mathrm{OH}^-$、$\mathrm{H}_2\mathrm{O}$ $\mathrm{Ca}^{2+}$、$\mathrm{OH}^-$、$\mathrm{H}_2\mathrm{O}$ $\mathrm{OH}^-$
3. 经研究表明,碱溶液具有一些相似的化学性质,如:
① 碱溶液都有碱性,都能使指示剂变色(如能使紫色石蕊溶液变
② 都能与二氧化碳等酸性非金属氧化物发生反应,生成
③ 都能与硫酸铜等盐溶液反应生成
① 碱溶液都有碱性,都能使指示剂变色(如能使紫色石蕊溶液变
蓝
,使无色酚酞溶液变红
)。② 都能与二氧化碳等酸性非金属氧化物发生反应,生成
盐
和水
。③ 都能与硫酸铜等盐溶液反应生成
新盐
和新碱
。答案:3.蓝 红 盐 水 新盐 新碱
1. 下列物质间发生反应时,属于复分解反应的是 (
A.镁条与稀盐酸
B.氢氧化钠溶液与硫酸铜溶液
C.石灰水与二氧化碳
D.氧化钙与水
B
)A.镁条与稀盐酸
B.氢氧化钠溶液与硫酸铜溶液
C.石灰水与二氧化碳
D.氧化钙与水
答案:1.B
2. 下列物质按单质、氧化物、酸、碱的顺序排列的是 (
A.碳、氧化铜、二氧化碳、氢氧化钠
B.氧气、氧化铁、碳酸、碳酸钠
C.氮气、氧化钙、硝酸、熟石灰
D.铁、一氧化碳、碳酸钙、氢氧化铜
C
)A.碳、氧化铜、二氧化碳、氢氧化钠
B.氧气、氧化铁、碳酸、碳酸钠
C.氮气、氧化钙、硝酸、熟石灰
D.铁、一氧化碳、碳酸钙、氢氧化铜
答案:2.C
3. “宏观辨识与微观探析”是化学学科的核心素养之一。下列解释不合理的是 (
A.镁原子和镁离子属于同种元素——它们原子核内的质子数或核电荷数相同
B.氢氧化钠与氢氧化钾都可与硫酸铜溶液反应——它们的溶液中均含有 $ \mathrm{OH}^{-} $
C.化学反应前后各物质的质量总和不变——反应前后原子的种类、数目、质量均不变
D.金刚石和石墨的物理性质不同——构成它们的微观粒子不同
D
)A.镁原子和镁离子属于同种元素——它们原子核内的质子数或核电荷数相同
B.氢氧化钠与氢氧化钾都可与硫酸铜溶液反应——它们的溶液中均含有 $ \mathrm{OH}^{-} $
C.化学反应前后各物质的质量总和不变——反应前后原子的种类、数目、质量均不变
D.金刚石和石墨的物理性质不同——构成它们的微观粒子不同
答案:3.D
4. 掌握物质的性质和用途,可以为人类开启智慧之旅。下列有关物质用途的叙述中,错误的是 (
A.用熟石灰配制波尔多液
B.用熟石灰改良酸性土壤
C.用 $ \mathrm{NaOH} $ 溶液检验 $ \mathrm{CO}_{2} $
D.用 $ \mathrm{NaOH} $ 制造碱性清洁剂、肥皂等
C
)A.用熟石灰配制波尔多液
B.用熟石灰改良酸性土壤
C.用 $ \mathrm{NaOH} $ 溶液检验 $ \mathrm{CO}_{2} $
D.用 $ \mathrm{NaOH} $ 制造碱性清洁剂、肥皂等
答案:4.C
5. 氧化钙俗称生石灰,某同学针对氧化钙设计了如下页图所示实验方案:
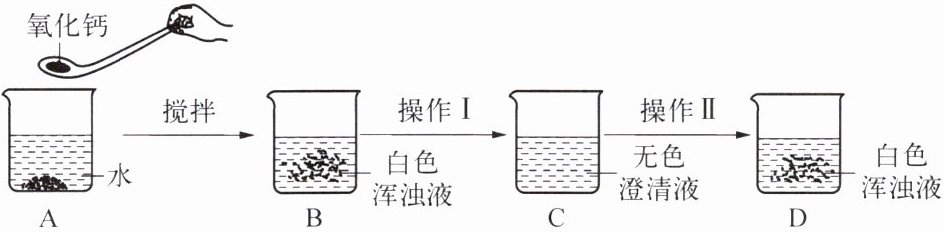
(1) A 中发生反应的化学方程式为
(2) 分离 B 中难溶物的操作 I 称为
(3) 如果要用实验证明 C 中不是水而是一种溶液,可以选择下列
① 稀盐酸 ② 酚酞溶液 ③ 二氧化碳 ④ 氯化钠溶液
(4) 操作 II 是加入某种物质后使无色澄清液中出现白色固体。如果加入的是碳酸钠溶液,白色固体的化学式是
(5) C 在空气中放置一段时间会变质,原因是

(1) A 中发生反应的化学方程式为
$\mathrm{CaO} + \mathrm{H}_2\mathrm{O} = \mathrm{Ca(OH)}_2$
。(2) 分离 B 中难溶物的操作 I 称为
过滤
。(3) 如果要用实验证明 C 中不是水而是一种溶液,可以选择下列
②③
(填序号)进行试验。① 稀盐酸 ② 酚酞溶液 ③ 二氧化碳 ④ 氯化钠溶液
(4) 操作 II 是加入某种物质后使无色澄清液中出现白色固体。如果加入的是碳酸钠溶液,白色固体的化学式是
$\mathrm{CaCO}_3$
,形成的原因是$\mathrm{Ca(OH)}_2 + \mathrm{Na}_2\mathrm{CO}_3 = \mathrm{CaCO}_3\downarrow + 2\mathrm{NaOH}$
(写化学方程式)。如果加入的是固体氢氧化钠(全部溶解),则白色固体是熟石灰(或消石灰)
(填俗称),形成的原因是固体氢氧化钠溶解时放出热量,使氢氧化钙的溶解度减小
。(5) C 在空气中放置一段时间会变质,原因是
$\mathrm{CO}_2 + \mathrm{Ca(OH)}_2 = \mathrm{CaCO}_3\downarrow + \mathrm{H}_2\mathrm{O}$
(写化学方程式)。答案:5.(1)$\mathrm{CaO} + \mathrm{H}_2\mathrm{O} = \mathrm{Ca(OH)}_2$ (2)过滤 (3)②③ (4)$\mathrm{CaCO}_3$ $\mathrm{Ca(OH)}_2 + \mathrm{Na}_2\mathrm{CO}_3 = \mathrm{CaCO}_3\downarrow + 2\mathrm{NaOH}$ 熟石灰(或消石灰) 固体氢氧化钠溶解时放出热量,使氢氧化钙的溶解度减小 (5)$\mathrm{CO}_2 + \mathrm{Ca(OH)}_2 = \mathrm{CaCO}_3\downarrow + \mathrm{H}_2\mathrm{O}$