1. 经实验可知,氢氧化钠溶液能与盐酸反应,反应时
放出
(填“放出”或“吸收”)热量。当滴入的盐酸量较少时,溶液中氢氧化钠
有剩余,溶液呈碱
性;当滴入的盐酸与氢氧化钠恰好完全反应时,溶液呈中
性;当滴入的盐酸过量时,溶液中盐酸
有剩余,溶液呈酸
性。盐酸与氢氧化钠溶液完全反应的结果是酸和碱各自的特性都消失,生成氯化钠
和水
。答案:1 放出 氢氧化钠 碱 中 盐酸 酸 氯化钠 水
2. 酸与碱作用生成盐和水的反应称为
中和
反应。它属于
(填“属于”或“不属于”)复分解反应。答案:2 中和 属于
3. 中和反应在生产、生活中有诸多应用。如:工业上,在硫酸厂的酸性废水中可以通过加入
熟石灰
以中和酸性,该反应的化学方程式为$\mathrm{Ca(OH)}_2 + \mathrm{H}_2\mathrm{SO}_4 \longrightarrow \mathrm{CaSO}_4 + 2\mathrm{H}_2\mathrm{O}$
;医疗上,可以使用含碱的药物(如氢氧化铝
)来中和胃酸,缓解胃酸过多引起的不适,该反应的化学方程式为$\mathrm{Al(OH)}_3 + 3\mathrm{HCl} \longrightarrow \mathrm{AlCl}_3 + 3\mathrm{H}_2\mathrm{O}$
;生活中可以使用洁厕灵(主要成分是盐酸
)或食醋清理下水道的水垢(水垢中含有氢氧化镁等难溶物);农业上,可以通过加入熟石灰
治理土壤酸化,保障农作物正常生长。答案:3 熟石灰 $\mathrm{Ca(OH)}_2 + \mathrm{H}_2\mathrm{SO}_4 \longrightarrow \mathrm{CaSO}_4 + 2\mathrm{H}_2\mathrm{O}$ 氢氧化铝 $\mathrm{Al(OH)}_3 + 3\mathrm{HCl} \longrightarrow \mathrm{AlCl}_3 + 3\mathrm{H}_2\mathrm{O}$ 盐酸 熟石灰
1. 下列有关中和反应的叙述中,正确的是(
A.中和反应一定有氧化物生成
B.中和反应不一定属于复分解反应
C.中和反应一定没有明显现象
D.中和反应不一定是放热反应
A
)A.中和反应一定有氧化物生成
B.中和反应不一定属于复分解反应
C.中和反应一定没有明显现象
D.中和反应不一定是放热反应
答案:1 A
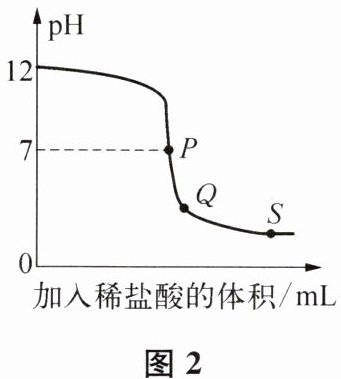
2. 常温下,某小组同学向氢氧化钠溶液 a 中加入水,向氢氧化钠溶液 b 中逐滴加入稀盐酸,利用 pH 传感器分别测得溶液 pH 的变化如图 1、图 2 所示。下列说法正确的是(
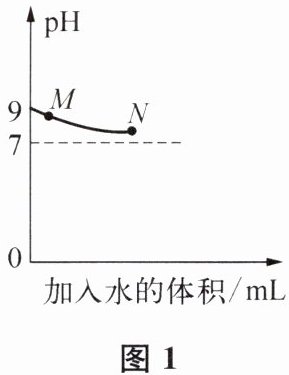
A.图 1:M 点时的溶液能使紫色石蕊溶液变红
B.图 1:向 N 点时的溶液中加大量水可使溶液的 pH≈6
C.图 2:向 P 点时的溶液中加入锌粒能产生气泡
D.图 2:Q→S 过程中,溶液中氯化钠的质量分数逐渐减小
D
)

A.图 1:M 点时的溶液能使紫色石蕊溶液变红
B.图 1:向 N 点时的溶液中加大量水可使溶液的 pH≈6
C.图 2:向 P 点时的溶液中加入锌粒能产生气泡
D.图 2:Q→S 过程中,溶液中氯化钠的质量分数逐渐减小
答案:2 D