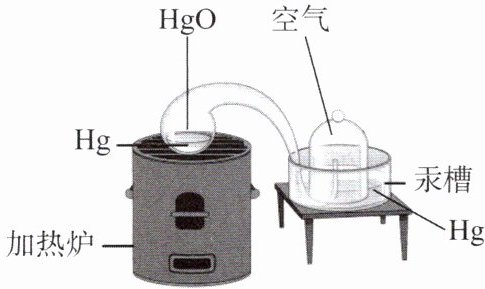
7. 在不同温度下,${Hg}与{HgO}$可以相互转化。如右图所示的实验装置可用来研究氧化汞的分解反应前后各物质的质量关系。下列叙述错误的是(
A.常温下,${Hg}很难与{O_{2}}$反应
B.汞在汞槽中起到液封的作用
C.汞能将密闭容器内空气中的氧气几乎耗尽
D.${HgO}$受热分解时,反应前后物质的总质量减少
D
)。
A.常温下,${Hg}很难与{O_{2}}$反应
B.汞在汞槽中起到液封的作用
C.汞能将密闭容器内空气中的氧气几乎耗尽
D.${HgO}$受热分解时,反应前后物质的总质量减少
答案:【解析】:
A. 常温下,汞(Hg)很难与氧气($O_2$)反应,这是汞的化学性质之一,故A选项正确。
B. 汞在汞槽中确实起到液封的作用,防止外界空气进入影响实验结果,故B选项正确。
C. 汞在加热条件下可以与氧气反应,但由于实验装置中空气是有限的,汞并不能将密闭容器内空气中的氧气几乎耗尽,但在该实验条件下,汞能与有限空气中的氧气反应,从而用于研究氧化汞分解前后物质质量关系,该选项从汞的性质和实验用途角度来说,表述合理,故C选项正确。
D. 根据质量守恒定律,化学反应前后物质的总质量是不变的。因此,氧化汞(HgO)受热分解时,反应前后物质的总质量应该保持不变,而不是减少,故D选项错误。
【答案】:D
A. 常温下,汞(Hg)很难与氧气($O_2$)反应,这是汞的化学性质之一,故A选项正确。
B. 汞在汞槽中确实起到液封的作用,防止外界空气进入影响实验结果,故B选项正确。
C. 汞在加热条件下可以与氧气反应,但由于实验装置中空气是有限的,汞并不能将密闭容器内空气中的氧气几乎耗尽,但在该实验条件下,汞能与有限空气中的氧气反应,从而用于研究氧化汞分解前后物质质量关系,该选项从汞的性质和实验用途角度来说,表述合理,故C选项正确。
D. 根据质量守恒定律,化学反应前后物质的总质量是不变的。因此,氧化汞(HgO)受热分解时,反应前后物质的总质量应该保持不变,而不是减少,故D选项错误。
【答案】:D
8. 一定量的镁条在空气中完全燃烧后,生成的固体的质量
大于
(选填“大于”“小于”或“等于”)镁条的质量,这符合
(选填“符合”或“不符合”)质量守恒定律。答案:【解析】:
本题主要考察质量守恒定律的应用。
质量守恒定律是化学反应中的基本定律,它表明在化学反应中,参加反应的各物质的质量总和等于反应后生成的各物质的质量总和。
镁条在空气中燃烧,是与空气中的氧气发生化学反应,生成氧化镁。根据质量守恒定律,参加反应的镁和氧气的质量之和应等于生成的氧化镁的质量。
因此,生成的氧化镁的质量必然大于参加反应的镁条的质量,因为还包含了与镁反应的氧气的质量。
这个现象完全符合质量守恒定律。
【答案】:
大于;符合。
本题主要考察质量守恒定律的应用。
质量守恒定律是化学反应中的基本定律,它表明在化学反应中,参加反应的各物质的质量总和等于反应后生成的各物质的质量总和。
镁条在空气中燃烧,是与空气中的氧气发生化学反应,生成氧化镁。根据质量守恒定律,参加反应的镁和氧气的质量之和应等于生成的氧化镁的质量。
因此,生成的氧化镁的质量必然大于参加反应的镁条的质量,因为还包含了与镁反应的氧气的质量。
这个现象完全符合质量守恒定律。
【答案】:
大于;符合。
9. 在反应${A\xlongequal{}B + C}$中,A分解生成了20 g B和8 g C,那么参加反应的A的质量是
28
g。答案:【解析】:本题考查质量守恒定律的应用。在化学反应中,参加反应的各物质的质量总和等于反应后生成的各物质的质量总和。根据题目描述,A分解生成了$20g$ B和$8g$ C,那么参加反应的A的质量就等于生成的B和C的质量之和。
【答案】:28
【答案】:28
10. 有一化学反应${R + 2O_{2}\xlongequal{}2CO_{2} + H_{2}O}$,那么R一定含有
对于反应${A + B\xlongequal{}C + D}$,生成物C和D的质量比为1∶3,若反应物A与B在反应中一共消耗2.4 g。则生成物中C的质量为
C、H
元素。对于反应${A + B\xlongequal{}C + D}$,生成物C和D的质量比为1∶3,若反应物A与B在反应中一共消耗2.4 g。则生成物中C的质量为
0.6
g,D的质量为1.8
g。答案:解:根据质量守恒定律,化学反应前后元素种类不变。反应后有C、H、O元素,氧气提供O元素,故R一定含有C、H元素。
解:由质量守恒定律,C和D的总质量为2.4g。设C的质量为x,则D的质量为3x,x+3x=2.4g,x=0.6g,3x=1.8g。
C、H;0.6;1.8
解:由质量守恒定律,C和D的总质量为2.4g。设C的质量为x,则D的质量为3x,x+3x=2.4g,x=0.6g,3x=1.8g。
C、H;0.6;1.8
11. 利用如右图所示装置进行如下实验探究。
在锥形瓶中放入一小粒白磷,塞好瓶塞后玻璃管下端刚好能与白磷接触,将整套装置放在托盘天平上调节至平衡。取下橡皮塞,将玻璃管放在酒精灯火焰上灼烧至红热,迅速塞紧瓶塞,将白磷引燃,待锥形瓶冷却后观察天平是否平衡。

(1)实验时,气球的变化为______
(2)实验前后天平保持平衡。实验后,松开橡皮塞,则天平指针______
在锥形瓶中放入一小粒白磷,塞好瓶塞后玻璃管下端刚好能与白磷接触,将整套装置放在托盘天平上调节至平衡。取下橡皮塞,将玻璃管放在酒精灯火焰上灼烧至红热,迅速塞紧瓶塞,将白磷引燃,待锥形瓶冷却后观察天平是否平衡。

(1)实验时,气球的变化为______
先膨胀后缩小
。(2)实验前后天平保持平衡。实验后,松开橡皮塞,则天平指针______
向左偏
(选填“向左偏”“向右偏”或“指向中间”)。答案:
(1)先膨胀后缩小
(2)向左偏
(1)先膨胀后缩小
(2)向左偏