1. 下列现象不能用质量守恒定律解释的是(
A.木炭燃烧后变成灰烬,质量减小
B.磷燃烧后生成的白烟比磷的质量大
C.酒精长时间敞口放置,质量逐渐减小
D.大理石和稀盐酸在敞口容器中反应后,剩余物总质量小于反应物总质量
C
)。A.木炭燃烧后变成灰烬,质量减小
B.磷燃烧后生成的白烟比磷的质量大
C.酒精长时间敞口放置,质量逐渐减小
D.大理石和稀盐酸在敞口容器中反应后,剩余物总质量小于反应物总质量
答案:【解析】:
本题主要考察质量守恒定律的适用范围。质量守恒定律是化学反应中的基本定律之一,它表明在化学反应中,参加反应的各物质的质量总和等于反应后生成的各物质的质量总和。这一定律只适用于化学变化,对于物理变化则不适用。
A选项描述的是木炭燃烧后变成灰烬,质量减小。这是一个化学变化过程,因为木炭燃烧生成了二氧化碳和水蒸气等新物质,同时部分质量以热能的形式散失,所以质量减小。这可以用质量守恒定律来解释。
B选项描述的是磷燃烧后生成的白烟比磷的质量大。这也是一个化学变化过程,磷燃烧生成了五氧化二磷固体小颗粒(白烟),由于参加反应的氧气质量也计算在内,所以生成的白烟质量比磷的质量大。这同样可以用质量守恒定律来解释。
C选项描述的是酒精长时间敞口放置,质量逐渐减小。这是一个物理变化过程,因为酒精只是从液态变为气态,没有新物质生成。这个过程不能用质量守恒定律来解释,因为质量守恒定律只适用于化学变化。
D选项描述的是大理石和稀盐酸在敞口容器中反应后,剩余物总质量小于反应物总质量。这是一个化学变化过程,大理石(碳酸钙)与稀盐酸反应生成了氯化钙、水和二氧化碳,由于二氧化碳以气态形式逸出,所以剩余物总质量小于反应物总质量。这可以用质量守恒定律来解释。
【答案】:C
本题主要考察质量守恒定律的适用范围。质量守恒定律是化学反应中的基本定律之一,它表明在化学反应中,参加反应的各物质的质量总和等于反应后生成的各物质的质量总和。这一定律只适用于化学变化,对于物理变化则不适用。
A选项描述的是木炭燃烧后变成灰烬,质量减小。这是一个化学变化过程,因为木炭燃烧生成了二氧化碳和水蒸气等新物质,同时部分质量以热能的形式散失,所以质量减小。这可以用质量守恒定律来解释。
B选项描述的是磷燃烧后生成的白烟比磷的质量大。这也是一个化学变化过程,磷燃烧生成了五氧化二磷固体小颗粒(白烟),由于参加反应的氧气质量也计算在内,所以生成的白烟质量比磷的质量大。这同样可以用质量守恒定律来解释。
C选项描述的是酒精长时间敞口放置,质量逐渐减小。这是一个物理变化过程,因为酒精只是从液态变为气态,没有新物质生成。这个过程不能用质量守恒定律来解释,因为质量守恒定律只适用于化学变化。
D选项描述的是大理石和稀盐酸在敞口容器中反应后,剩余物总质量小于反应物总质量。这是一个化学变化过程,大理石(碳酸钙)与稀盐酸反应生成了氯化钙、水和二氧化碳,由于二氧化碳以气态形式逸出,所以剩余物总质量小于反应物总质量。这可以用质量守恒定律来解释。
【答案】:C
2. 液态物质X和过氧化氢可为火箭提供动力,当它们混合反应时,放出大量的热,产生强大的推动力。有关反应的化学方程式为:${X + 2H_{2}O_{2}\xlongequal{}N_{2}\uparrow + 4H_{2}O}$,则X的化学式为(
A.${NH_{3}}$
B.${N_{2}O_{4}}$
C.${NO_{2}}$
D.${N_{2}H_{4}}$
D
)。A.${NH_{3}}$
B.${N_{2}O_{4}}$
C.${NO_{2}}$
D.${N_{2}H_{4}}$
答案:【解析】:
根据题目中的化学方程式 $X + 2H_2O_2 \rightarrow N_2 \uparrow + 4H_2O$,需要确定X的化学式。首先,根据质量守恒定律,反应前后各元素的原子数目必须相等。
反应产物中有:
氮(N)原子:2个(来自 $N_2$),
氢(H)原子:8个(来自 $4H_2O$),
氧(O)原子:4个(来自 $4H_2O$)。
反应物中有:
过氧化氢 $2H_2O_2$ 提供氢(H)原子:4个,氧(O)原子:4个。
因此,X中必须包含2个氮原子和4个氢原子,以满足氮和氢的原子守恒。
选项分析:
A. $NH_3$:1个氮原子,3个氢原子,不符合。
B. $N_2O_4$:2个氮原子,4个氧原子,不符合。
C. $NO_2$:1个氮原子,2个氧原子,不符合。
D. $N_2H_4$:2个氮原子,4个氢原子,符合。
故D选项正确。
【答案】:D
根据题目中的化学方程式 $X + 2H_2O_2 \rightarrow N_2 \uparrow + 4H_2O$,需要确定X的化学式。首先,根据质量守恒定律,反应前后各元素的原子数目必须相等。
反应产物中有:
氮(N)原子:2个(来自 $N_2$),
氢(H)原子:8个(来自 $4H_2O$),
氧(O)原子:4个(来自 $4H_2O$)。
反应物中有:
过氧化氢 $2H_2O_2$ 提供氢(H)原子:4个,氧(O)原子:4个。
因此,X中必须包含2个氮原子和4个氢原子,以满足氮和氢的原子守恒。
选项分析:
A. $NH_3$:1个氮原子,3个氢原子,不符合。
B. $N_2O_4$:2个氮原子,4个氧原子,不符合。
C. $NO_2$:1个氮原子,2个氧原子,不符合。
D. $N_2H_4$:2个氮原子,4个氢原子,符合。
故D选项正确。
【答案】:D
3. 某物质在密闭容器中隔绝空气分解,生成了二氧化碳和水,这一实验说明了(
A.该物质必定是由碳、氢、氧三种元素组成的
B.该物质分子是由碳原子和水分子构成的
C.该物质是炭黑和水组成的混合物
D.该物质可能是由碳元素和氢元素组成的纯净物
A
)。A.该物质必定是由碳、氢、氧三种元素组成的
B.该物质分子是由碳原子和水分子构成的
C.该物质是炭黑和水组成的混合物
D.该物质可能是由碳元素和氢元素组成的纯净物
答案:【解析】:本题主要考查了质量守恒定律的应用以及物质的组成和构成。
A选项,根据质量守恒定律,化学反应前后,元素的种类不变。某物质在密闭容器中隔绝空气分解,生成了二氧化碳和水,二氧化碳中的碳元素和水中的氢元素一定来自于该物质,同时,由于该物质在密闭容器中分解,没有外界氧元素的参与,因此可以推断出该物质中一定含有碳元素和氢元素,而氧元素可能来自于该物质本身,也可能部分或全部来自于反应中的其他物质(如可能存在的含氧杂质或反应中生成的氧气等,但在此题情境下,我们主要关注该物质本身的组成)。然而,由于题目中明确指出是“隔绝空气分解”,且生成了二氧化碳和水,因此可以合理推断出该物质中必定含有氧元素,否则无法生成这两种含氧化合物。所以,该物质必定是由碳、氢、氧三种元素组成的,A选项正确。
B选项,分子是由原子构成的,而不是由其他分子构成的。因此,该物质的分子不可能由碳原子和水分子构成,B选项错误。
C选项,该物质在密闭容器中分解生成了二氧化碳和水,说明它是一种化合物,而不是混合物。炭黑和水是两种不同的物质,它们组成的混合物不可能在密闭容器中分解生成二氧化碳和水,C选项错误。
D选项,虽然该物质一定含有碳元素和氢元素,但由于生成了含氧化合物,因此它不可能只是由碳元素和氢元素组成的纯净物,还必须含有氧元素。所以D选项错误。
【答案】:A
A选项,根据质量守恒定律,化学反应前后,元素的种类不变。某物质在密闭容器中隔绝空气分解,生成了二氧化碳和水,二氧化碳中的碳元素和水中的氢元素一定来自于该物质,同时,由于该物质在密闭容器中分解,没有外界氧元素的参与,因此可以推断出该物质中一定含有碳元素和氢元素,而氧元素可能来自于该物质本身,也可能部分或全部来自于反应中的其他物质(如可能存在的含氧杂质或反应中生成的氧气等,但在此题情境下,我们主要关注该物质本身的组成)。然而,由于题目中明确指出是“隔绝空气分解”,且生成了二氧化碳和水,因此可以合理推断出该物质中必定含有氧元素,否则无法生成这两种含氧化合物。所以,该物质必定是由碳、氢、氧三种元素组成的,A选项正确。
B选项,分子是由原子构成的,而不是由其他分子构成的。因此,该物质的分子不可能由碳原子和水分子构成,B选项错误。
C选项,该物质在密闭容器中分解生成了二氧化碳和水,说明它是一种化合物,而不是混合物。炭黑和水是两种不同的物质,它们组成的混合物不可能在密闭容器中分解生成二氧化碳和水,C选项错误。
D选项,虽然该物质一定含有碳元素和氢元素,但由于生成了含氧化合物,因此它不可能只是由碳元素和氢元素组成的纯净物,还必须含有氧元素。所以D选项错误。
【答案】:A
4. a g白磷在b g氧气中恰好完全燃烧,同时生成c g五氧化二磷,下列叙述不正确的是(
A.a与b之和等于c
B.反应前后磷元素和氧元素种类不变
C.反应前后分子总数不变
D.反应前后磷原子总数和氧原子总数不变
C
)。A.a与b之和等于c
B.反应前后磷元素和氧元素种类不变
C.反应前后分子总数不变
D.反应前后磷原子总数和氧原子总数不变
答案:【解析】:
本题主要考察质量守恒定律及其应用。
A选项:根据质量守恒定律,参加化学反应的各物质的质量总和等于反应后生成的各物质的质量总和。因此,a g白磷与b g氧气恰好完全反应,生成的c g五氧化二磷的质量应等于a g与b g之和,即$a+b=c$。所以A选项正确。
B选项:根据质量守恒定律的微观解释,化学反应前后,元素的种类是不变的。因此,反应前后磷元素和氧元素的种类不变。所以B选项正确。
C选项:需要具体看反应方程式$4P + 5O_{2} \overset{点燃}=2P_{2}O_{5}$,可以看出反应前分子总数为$4+5=9$,而反应后分子总数为2,因此反应前后分子总数是改变的。所以C选项错误。
D选项:根据质量守恒定律的微观解释,化学反应前后,原子的种类、数目、质量都是不变的。因此,反应前后磷原子总数和氧原子总数不变。所以D选项正确。
【答案】:C
本题主要考察质量守恒定律及其应用。
A选项:根据质量守恒定律,参加化学反应的各物质的质量总和等于反应后生成的各物质的质量总和。因此,a g白磷与b g氧气恰好完全反应,生成的c g五氧化二磷的质量应等于a g与b g之和,即$a+b=c$。所以A选项正确。
B选项:根据质量守恒定律的微观解释,化学反应前后,元素的种类是不变的。因此,反应前后磷元素和氧元素的种类不变。所以B选项正确。
C选项:需要具体看反应方程式$4P + 5O_{2} \overset{点燃}=2P_{2}O_{5}$,可以看出反应前分子总数为$4+5=9$,而反应后分子总数为2,因此反应前后分子总数是改变的。所以C选项错误。
D选项:根据质量守恒定律的微观解释,化学反应前后,原子的种类、数目、质量都是不变的。因此,反应前后磷原子总数和氧原子总数不变。所以D选项正确。
【答案】:C
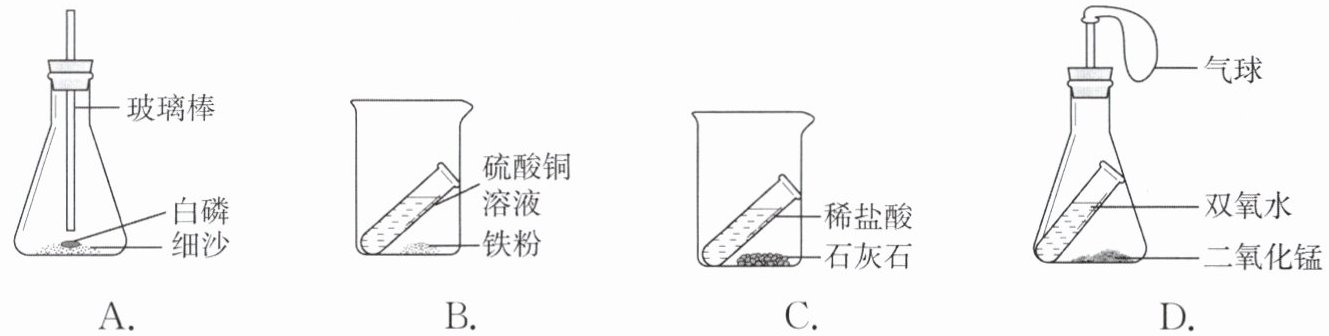
5. 用下列装置进行验证质量守恒定律的实验,反应前后容器中物质的总质量不相等的是(
A.
B.
C.
D.
C
)。
A.
B.
C.
D.
答案:【解析】:
A选项:白磷在密闭的锥形瓶中燃烧,反应前后物质都在锥形瓶中,总质量不变,能验证质量守恒定律。
B选项:铁粉与硫酸铜溶液在敞口烧杯中反应,没有气体参与和生成,反应前后物质都在烧杯中,总质量不变,能验证质量守恒定律。
C选项:石灰石(主要成分碳酸钙)与稀盐酸反应会生成二氧化碳气体,该装置是敞口的,生成的二氧化碳气体会逸散到空气中,导致反应后容器中物质的总质量减小,不能验证质量守恒定律。
D选项:过氧化氢在二氧化锰的催化作用下分解生成水和氧气,但装置是密闭的,氧气不会逸出,反应前后总质量不变,能验证质量守恒定律。
【答案】:C
A选项:白磷在密闭的锥形瓶中燃烧,反应前后物质都在锥形瓶中,总质量不变,能验证质量守恒定律。
B选项:铁粉与硫酸铜溶液在敞口烧杯中反应,没有气体参与和生成,反应前后物质都在烧杯中,总质量不变,能验证质量守恒定律。
C选项:石灰石(主要成分碳酸钙)与稀盐酸反应会生成二氧化碳气体,该装置是敞口的,生成的二氧化碳气体会逸散到空气中,导致反应后容器中物质的总质量减小,不能验证质量守恒定律。
D选项:过氧化氢在二氧化锰的催化作用下分解生成水和氧气,但装置是密闭的,氧气不会逸出,反应前后总质量不变,能验证质量守恒定律。
【答案】:C
6. 下列各项中,化学反应前后肯定没有变化的是(
①原子的数目 ②元素的种类 ③物质的总质量 ④物质的种类 ⑤原子的种类 ⑥分子的种类
A.①②③④⑤⑥
B.仅①②③⑤
C.仅①②③④⑤
D.仅③④⑤⑥
B
)。①原子的数目 ②元素的种类 ③物质的总质量 ④物质的种类 ⑤原子的种类 ⑥分子的种类
A.①②③④⑤⑥
B.仅①②③⑤
C.仅①②③④⑤
D.仅③④⑤⑥
答案:【解析】:
本题考查的是化学反应中质量守恒定律的理解及应用。在化学反应中,遵循质量守恒定律,即反应前后,原子的种类、数目、质量均不变,因此元素的种类也不会改变,物质的总质量也保持不变。这是解答此题的关键知识点。
接下来,我们逐一分析每个选项:
①原子的数目:在化学反应中,原子是化学反应中的最小粒子,其数目在反应前后是不变的,所以①是正确的。
②元素的种类:由于化学反应中,原子种类不变,因此元素种类也不会改变,所以②是正确的。
③物质的总质量:根据质量守恒定律,化学反应前后物质的总质量是不变的,所以③是正确的。
④物质的种类:化学反应的本质就是物质的种类发生改变,所以④是错误的。
⑤原子的种类:化学反应中,原子种类是不变的,所以⑤是正确的。
⑥分子的种类:化学反应中,分子的种类是会发生改变的,因为化学反应就是旧化学键的断裂和新化学键的形成,所以⑥是错误的。
综上所述,化学反应前后肯定没有变化的是①原子的数目、②元素的种类、③物质的总质量、⑤原子的种类,所以正确答案是B。
【答案】:B
本题考查的是化学反应中质量守恒定律的理解及应用。在化学反应中,遵循质量守恒定律,即反应前后,原子的种类、数目、质量均不变,因此元素的种类也不会改变,物质的总质量也保持不变。这是解答此题的关键知识点。
接下来,我们逐一分析每个选项:
①原子的数目:在化学反应中,原子是化学反应中的最小粒子,其数目在反应前后是不变的,所以①是正确的。
②元素的种类:由于化学反应中,原子种类不变,因此元素种类也不会改变,所以②是正确的。
③物质的总质量:根据质量守恒定律,化学反应前后物质的总质量是不变的,所以③是正确的。
④物质的种类:化学反应的本质就是物质的种类发生改变,所以④是错误的。
⑤原子的种类:化学反应中,原子种类是不变的,所以⑤是正确的。
⑥分子的种类:化学反应中,分子的种类是会发生改变的,因为化学反应就是旧化学键的断裂和新化学键的形成,所以⑥是错误的。
综上所述,化学反应前后肯定没有变化的是①原子的数目、②元素的种类、③物质的总质量、⑤原子的种类,所以正确答案是B。
【答案】:B