1. 铁和铜都会被腐蚀,下列不能说明铁比铜活泼的事实是(
A.历史上铜比铁使用更早
B.铁的文物比铜的稀有
C.铁能被磁铁吸引而铜不能
D.铁能与硫酸铜溶液反应
C
)。A.历史上铜比铁使用更早
B.铁的文物比铜的稀有
C.铁能被磁铁吸引而铜不能
D.铁能与硫酸铜溶液反应
答案:【解析】:
本题主要考察金属活动性的判断依据。
A选项,金属的使用先后顺序可以反映金属的活动性强弱,活动性弱的金属由于更稳定,往往更早被人类使用,铜比铁早使用,说明铜的活动性比铁弱,故A选项能说明铁比铜活泼。
B选项,铁的文物比铜的稀有,说明铁由于活泼,更容易与空气中的氧气等物质反应而腐蚀,导致铁文物保存下来的较少,故B选项能说明铁比铜活泼。
C选项,铁能被磁铁吸引而铜不能,这是铁的物理性质,与金属的活动性无关,不能作为判断铁比铜活泼的依据,故C选项符合题意。
D选项,铁能与硫酸铜溶液反应,根据金属活动性顺序,排在前面的金属能把排在后面的金属从其盐溶液中置换出来,铁能置换出铜,说明铁比铜活泼,故D选项能说明铁比铜活泼。
【答案】:C
本题主要考察金属活动性的判断依据。
A选项,金属的使用先后顺序可以反映金属的活动性强弱,活动性弱的金属由于更稳定,往往更早被人类使用,铜比铁早使用,说明铜的活动性比铁弱,故A选项能说明铁比铜活泼。
B选项,铁的文物比铜的稀有,说明铁由于活泼,更容易与空气中的氧气等物质反应而腐蚀,导致铁文物保存下来的较少,故B选项能说明铁比铜活泼。
C选项,铁能被磁铁吸引而铜不能,这是铁的物理性质,与金属的活动性无关,不能作为判断铁比铜活泼的依据,故C选项符合题意。
D选项,铁能与硫酸铜溶液反应,根据金属活动性顺序,排在前面的金属能把排在后面的金属从其盐溶液中置换出来,铁能置换出铜,说明铁比铜活泼,故D选项能说明铁比铜活泼。
【答案】:C
2. 下列说法错误的是(
A.纯铁比生铁的硬度更小、熔点更高
B.我国在古代就掌握了湿法冶金技术
C.金属元素在自然界中大多以化合物形式存在
D.除去铁制品表面的油膜能更好地防止其被腐蚀
D
)。A.纯铁比生铁的硬度更小、熔点更高
B.我国在古代就掌握了湿法冶金技术
C.金属元素在自然界中大多以化合物形式存在
D.除去铁制品表面的油膜能更好地防止其被腐蚀
答案:【解析】:
A选项:纯铁与生铁的性质对比。纯铁是由铁元素单独组成,而生铁是铁和碳的合金。合金的硬度一般比其成分金属高,熔点则比成分金属低。因此,纯铁比生铁的硬度更小、熔点更高,A选项说法正确。
B选项:湿法冶金技术的历史。我国在古代就掌握了湿法冶金技术,如用铁与硫酸铜溶液反应制取铜,B选项说法正确。
C选项:金属元素在自然界中的存在形式。由于金属元素通常具有较强的还原性,容易与氧、硫等元素结合,因此在自然界中大多以化合物形式存在,C选项说法正确。
D选项:铁制品的防腐蚀措施。铁生锈的条件是与氧气和水同时接触。油膜可以隔绝氧气和水,从而防止铁制品生锈。因此,除去铁制品表面的油膜并不能更好地防止其被腐蚀,反而会增加生锈的风险,D选项说法错误。
【答案】:D
A选项:纯铁与生铁的性质对比。纯铁是由铁元素单独组成,而生铁是铁和碳的合金。合金的硬度一般比其成分金属高,熔点则比成分金属低。因此,纯铁比生铁的硬度更小、熔点更高,A选项说法正确。
B选项:湿法冶金技术的历史。我国在古代就掌握了湿法冶金技术,如用铁与硫酸铜溶液反应制取铜,B选项说法正确。
C选项:金属元素在自然界中的存在形式。由于金属元素通常具有较强的还原性,容易与氧、硫等元素结合,因此在自然界中大多以化合物形式存在,C选项说法正确。
D选项:铁制品的防腐蚀措施。铁生锈的条件是与氧气和水同时接触。油膜可以隔绝氧气和水,从而防止铁制品生锈。因此,除去铁制品表面的油膜并不能更好地防止其被腐蚀,反而会增加生锈的风险,D选项说法错误。
【答案】:D
3. 工业上冶炼钢铁的主要工艺流程如下,下列有关说法错误的是(
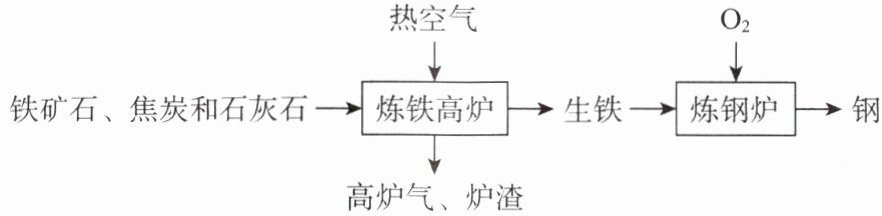
A.炼铁高炉中铁矿石中的主要成分发生置换反应生成铁
B.石灰石的作用是将铁矿石中的$SiO_2$转变为炉渣除去
C.炼钢炉中通入$O_2$的目的是降低生铁的含碳量
D.炼铁高炉中焦炭能提供热量和一氧化碳
A
)。
A.炼铁高炉中铁矿石中的主要成分发生置换反应生成铁
B.石灰石的作用是将铁矿石中的$SiO_2$转变为炉渣除去
C.炼钢炉中通入$O_2$的目的是降低生铁的含碳量
D.炼铁高炉中焦炭能提供热量和一氧化碳
答案:【解析】:
A选项:炼铁高炉中铁矿石中的主要成分是铁的氧化物,如$Fe_2O_3$,在还原剂(如一氧化碳)的作用下被还原成铁,但这不是置换反应,因为置换反应要求反应物中有单质参与,而这里主要是化合物之间的反应,故A选项错误。
B选项:石灰石在高温下分解生成氧化钙和二氧化碳,氧化钙与铁矿石中的$SiO_2$反应生成硅酸钙,即炉渣,从而将$SiO_2$除去,故B选项正确。
C选项:炼钢炉中通入氧气,氧气与生铁中的碳反应生成二氧化碳,从而降低生铁的含碳量,故C选项正确。
D选项:炼铁高炉中焦炭的作用有两个:一是燃烧提供热量,二是与氧气反应生成一氧化碳作为还原剂还原铁矿石,故D选项正确。
【答案】:A
A选项:炼铁高炉中铁矿石中的主要成分是铁的氧化物,如$Fe_2O_3$,在还原剂(如一氧化碳)的作用下被还原成铁,但这不是置换反应,因为置换反应要求反应物中有单质参与,而这里主要是化合物之间的反应,故A选项错误。
B选项:石灰石在高温下分解生成氧化钙和二氧化碳,氧化钙与铁矿石中的$SiO_2$反应生成硅酸钙,即炉渣,从而将$SiO_2$除去,故B选项正确。
C选项:炼钢炉中通入氧气,氧气与生铁中的碳反应生成二氧化碳,从而降低生铁的含碳量,故C选项正确。
D选项:炼铁高炉中焦炭的作用有两个:一是燃烧提供热量,二是与氧气反应生成一氧化碳作为还原剂还原铁矿石,故D选项正确。
【答案】:A
4. 下表为某次实验中氢气制备对比实验的数据(将锌粒压成薄锌片增大了表面积)。下列不能由实验得出的结论是(
|编号|20 mL硫酸的质量分数|1 g锌的形状|0~3 min产生氢气体积|
|①|20%|锌粒|31.7 mL|
|②|20%|薄锌片|50.9 mL|
|③|30%|锌粒|61.7 mL|
|④|30%|薄锌片|79.9 mL|

A.根据相同时间内产生氢气的多少,可比较反应速率的快慢
B.锌粒产生氢气的体积总是比薄锌片少
C.增大硫酸的质量分数能加快产生氢气
D.增大锌与酸的接触面积能加快产生氢气
B
)。|编号|20 mL硫酸的质量分数|1 g锌的形状|0~3 min产生氢气体积|
|①|20%|锌粒|31.7 mL|
|②|20%|薄锌片|50.9 mL|
|③|30%|锌粒|61.7 mL|
|④|30%|薄锌片|79.9 mL|

A.根据相同时间内产生氢气的多少,可比较反应速率的快慢
B.锌粒产生氢气的体积总是比薄锌片少
C.增大硫酸的质量分数能加快产生氢气
D.增大锌与酸的接触面积能加快产生氢气
答案:【解析】:
A选项:相同时间内产生氢气的体积越多,说明反应速率越快,该选项可以由实验得出。
B选项:从实验数据看,在相同硫酸质量分数下,锌粒产生氢气的体积比薄锌片少,但不同硫酸质量分数时不能简单得出此结论,比如①中锌粒产生氢气$31.7mL$,③中锌粒产生氢气$61.7mL$,而②中薄锌片产生氢气$50.9mL$,④中薄锌片产生氢气$79.9mL$,不能绝对地说锌粒产生氢气的体积总是比薄锌片少,该选项不能由实验得出。
C选项:对比①③或②④,硫酸质量分数从$20\%$增大到$30\%$,相同时间内产生氢气的体积增多,说明增大硫酸的质量分数能加快产生氢气,该选项可以由实验得出。
D选项:对比①②或③④,锌的形状从锌粒变为薄锌片,增大了与酸的接触面积,相同时间内产生氢气的体积增多,说明增大锌与酸的接触面积能加快产生氢气,该选项可以由实验得出。
答案:B
【答案】:B
A选项:相同时间内产生氢气的体积越多,说明反应速率越快,该选项可以由实验得出。
B选项:从实验数据看,在相同硫酸质量分数下,锌粒产生氢气的体积比薄锌片少,但不同硫酸质量分数时不能简单得出此结论,比如①中锌粒产生氢气$31.7mL$,③中锌粒产生氢气$61.7mL$,而②中薄锌片产生氢气$50.9mL$,④中薄锌片产生氢气$79.9mL$,不能绝对地说锌粒产生氢气的体积总是比薄锌片少,该选项不能由实验得出。
C选项:对比①③或②④,硫酸质量分数从$20\%$增大到$30\%$,相同时间内产生氢气的体积增多,说明增大硫酸的质量分数能加快产生氢气,该选项可以由实验得出。
D选项:对比①②或③④,锌的形状从锌粒变为薄锌片,增大了与酸的接触面积,相同时间内产生氢气的体积增多,说明增大锌与酸的接触面积能加快产生氢气,该选项可以由实验得出。
答案:B
【答案】:B