问题 1. 有关溶液中溶质的质量分数计算的注意事项有哪些?
要点 1. 计算过程中要保证单位统一。
2. 要分清加入物质和溶液中溶质、溶剂的关系。
① 加入物质没有完全溶解,即已形成饱和溶液,则计算溶质的质量分数时,不能以加入的质量进行计算,而应以饱和溶液中物质的溶解度计算。
② 加入物质如能与溶质或溶剂发生反应,则此时所计算的溶质的质量分数应为反应后生成物的溶质的质量分数。
3. 公式换算:溶质质量(m)=溶液质量×溶质的质量分数=溶液体积(V)×溶液密度(ρ)×溶质的质量分数。
应用 配制溶质的质量分数为 5%的下列溶液,能达到目的的是(
A. 称取 5.0 g 氯化钾,溶解在 95 mL 水中,充分搅拌
B. 称取 5.0 g 生石灰,放入 95 mL 水中,充分搅拌
C. 量取 5.0 mL 浓盐酸,倒入 95 mL 水中,充分搅拌
D. 称取 5.0 g 碳酸钙,放入 95 mL 水中,充分搅拌
要点 1. 计算过程中要保证单位统一。
2. 要分清加入物质和溶液中溶质、溶剂的关系。
① 加入物质没有完全溶解,即已形成饱和溶液,则计算溶质的质量分数时,不能以加入的质量进行计算,而应以饱和溶液中物质的溶解度计算。
② 加入物质如能与溶质或溶剂发生反应,则此时所计算的溶质的质量分数应为反应后生成物的溶质的质量分数。
3. 公式换算:溶质质量(m)=溶液质量×溶质的质量分数=溶液体积(V)×溶液密度(ρ)×溶质的质量分数。
应用 配制溶质的质量分数为 5%的下列溶液,能达到目的的是(
A
)A. 称取 5.0 g 氯化钾,溶解在 95 mL 水中,充分搅拌
B. 称取 5.0 g 生石灰,放入 95 mL 水中,充分搅拌
C. 量取 5.0 mL 浓盐酸,倒入 95 mL 水中,充分搅拌
D. 称取 5.0 g 碳酸钙,放入 95 mL 水中,充分搅拌
答案:问题1 应用:A
解析:
问题1 注意事项:
1. 计算过程中要保证单位统一。
2. 要分清加入物质和溶液中溶质、溶剂的关系。
① 加入物质没有完全溶解,即已形成饱和溶液,则计算溶质的质量分数时,不能以加入的质量进行计算,而应以饱和溶液中物质的溶解度计算。
② 加入物质如能与溶质或溶剂发生反应,则此时所计算的溶质的质量分数应为反应后生成物的溶质的质量分数。
3. 公式换算:溶质质量$(m)=$溶液质量$×$溶质的质量分数$=$溶液体积$(V)×$溶液密度$(\rho)×$溶质的质量分数。
应用:A
1. 计算过程中要保证单位统一。
2. 要分清加入物质和溶液中溶质、溶剂的关系。
① 加入物质没有完全溶解,即已形成饱和溶液,则计算溶质的质量分数时,不能以加入的质量进行计算,而应以饱和溶液中物质的溶解度计算。
② 加入物质如能与溶质或溶剂发生反应,则此时所计算的溶质的质量分数应为反应后生成物的溶质的质量分数。
3. 公式换算:溶质质量$(m)=$溶液质量$×$溶质的质量分数$=$溶液体积$(V)×$溶液密度$(\rho)×$溶质的质量分数。
应用:A
问题 2. 如何配制一定溶质的质量分数的溶液?
要点 1. 实验原理:用固体或浓溶液稀释配制成稀溶液,配制前后溶液中溶质的质量相等。
2. 配制过程。
① 计算:按配制要求计算出所需溶质和溶剂的量;② 称量和量取;③ 溶解;④ 装瓶贴标签。
应用 如图所示是小明配制 100 g 质量分数为 18.5%的蔗糖溶液的实验操作示意图。
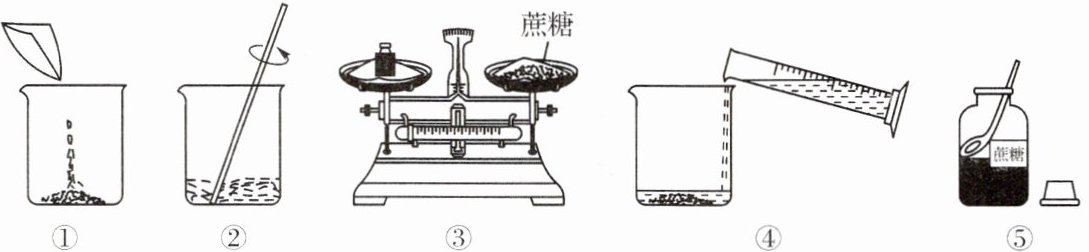
(1) 配制上述溶液,小明要称取蔗糖
(2) 上图①②④中相同的仪器名称是
(3) 用上图所示的序号表示正确配制该溶液的操作顺序:
(4) 若图③中砝码的质量为 15 g,游码的读数为 3.5 g,则小明称得的蔗糖质量实际为
要点 1. 实验原理:用固体或浓溶液稀释配制成稀溶液,配制前后溶液中溶质的质量相等。
2. 配制过程。
① 计算:按配制要求计算出所需溶质和溶剂的量;② 称量和量取;③ 溶解;④ 装瓶贴标签。
应用 如图所示是小明配制 100 g 质量分数为 18.5%的蔗糖溶液的实验操作示意图。

(1) 配制上述溶液,小明要称取蔗糖
18.5
g。(2) 上图①②④中相同的仪器名称是
烧杯
。(3) 用上图所示的序号表示正确配制该溶液的操作顺序:
⑤
→③
→①
→④
→②
。(4) 若图③中砝码的质量为 15 g,游码的读数为 3.5 g,则小明称得的蔗糖质量实际为
11.5
g。答案:问题2 应用:(1)18.5 (2)烧杯 (3)⑤ ③ ① ④ ② (4)11.5
问题 3. 如何去除粗盐中难溶性的杂质?
要点 1. 粗盐提纯过程中多次用到了玻璃棒,其作用分别为:溶解中能
2. 通过溶解、过滤、蒸发等操作,只除去了粗盐中的
应用 某兴趣小组按下列流程对含有泥沙的粗食盐进行提纯,请根据实验回答下列问题:

(1) 操作①②③都要用到的一种玻璃仪器是
(2) 操作②中需要将圆形滤纸折叠处理,下列图示中不该出现的情形是
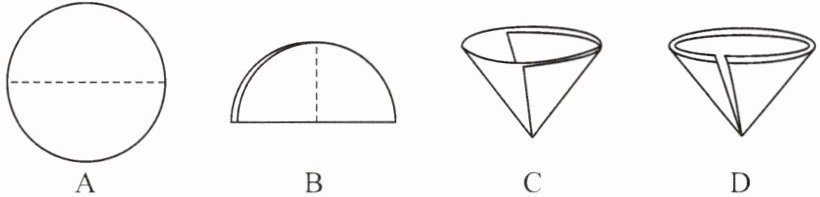
(3) 操作③中,当蒸发皿中
(4) 实验结束后称量获得的精盐,并计算精盐的产率,发现产率较低,其可能原因是
A. 过滤时滤纸有破损
B. 蒸发时有固体溅出
C. 溶解含有泥沙的粗食盐时,加入的水量不足
D. 蒸发后,所得精盐很潮湿
要点 1. 粗盐提纯过程中多次用到了玻璃棒,其作用分别为:溶解中能
加速溶解
、过滤中能引流
、蒸发中能使滤液受热均匀,防止局部过热
、计算产率时能移动固体
。2. 通过溶解、过滤、蒸发等操作,只除去了粗盐中的
不溶性
杂质,而氯化镁、氯化钙等可溶性
杂质并没有被除去。应用 某兴趣小组按下列流程对含有泥沙的粗食盐进行提纯,请根据实验回答下列问题:

(1) 操作①②③都要用到的一种玻璃仪器是
玻璃棒
。(2) 操作②中需要将圆形滤纸折叠处理,下列图示中不该出现的情形是
D
(填序号)。
(3) 操作③中,当蒸发皿中
出现大量晶体
时,停止加热。(4) 实验结束后称量获得的精盐,并计算精盐的产率,发现产率较低,其可能原因是
BC
(填字母序号)。A. 过滤时滤纸有破损
B. 蒸发时有固体溅出
C. 溶解含有泥沙的粗食盐时,加入的水量不足
D. 蒸发后,所得精盐很潮湿
答案:问题3 要点:1 加速溶解 引流 使滤液受热均匀,防止局部过热 移动固体 2 不溶性 可溶性 应用:(1)玻璃棒 (2)D (3)出现大量晶体 (4)BC