1. 人们通常把从溶液中析出晶体的过程称为
结晶
。结晶的方法有蒸发结晶
和降温结晶
。答案:1 结晶 蒸发结晶 降温结晶
2. 蒸发结晶一般适用于
溶解度随温度变化较小
的物质,如氯化钠
;降温结晶一般适用于溶解度随温度变化较大
的物质,如硝酸钾
。答案:2 溶解度随温度变化较小 氯化钠 溶解度随温度变化较大 硝酸钾
1. 要想从食盐溶液中得到食盐晶体,宜采取的方法是(
A.蒸发溶剂
B.冷却热饱和溶液
C.倒掉部分溶液
D.升高温度
A
)A.蒸发溶剂
B.冷却热饱和溶液
C.倒掉部分溶液
D.升高温度
答案:1 A
解析:
【解析】
食盐的主要成分是氯化钠,氯化钠的溶解度受温度变化影响较小。冷却热饱和溶液法适用于溶解度受温度影响较大的物质,无法有效从食盐溶液中得到晶体;倒掉部分溶液只是减少溶液量,不能得到食盐晶体;升高温度,氯化钠溶解度变化很小,也不能得到晶体。因此宜采取蒸发溶剂的方法,故选A。
【答案】
A
【知识点】
蒸发结晶、溶解度与温度的关系
【点评】
本题考查结晶方法的选择,需根据物质溶解度受温度影响的差异来判断不同结晶方法的适用场景,属于基础题型,帮助学生区分蒸发溶剂和冷却热饱和溶液法的应用条件。
【难度系数】
0.8
食盐的主要成分是氯化钠,氯化钠的溶解度受温度变化影响较小。冷却热饱和溶液法适用于溶解度受温度影响较大的物质,无法有效从食盐溶液中得到晶体;倒掉部分溶液只是减少溶液量,不能得到食盐晶体;升高温度,氯化钠溶解度变化很小,也不能得到晶体。因此宜采取蒸发溶剂的方法,故选A。
【答案】
A
【知识点】
蒸发结晶、溶解度与温度的关系
【点评】
本题考查结晶方法的选择,需根据物质溶解度受温度影响的差异来判断不同结晶方法的适用场景,属于基础题型,帮助学生区分蒸发溶剂和冷却热饱和溶液法的应用条件。
【难度系数】
0.8
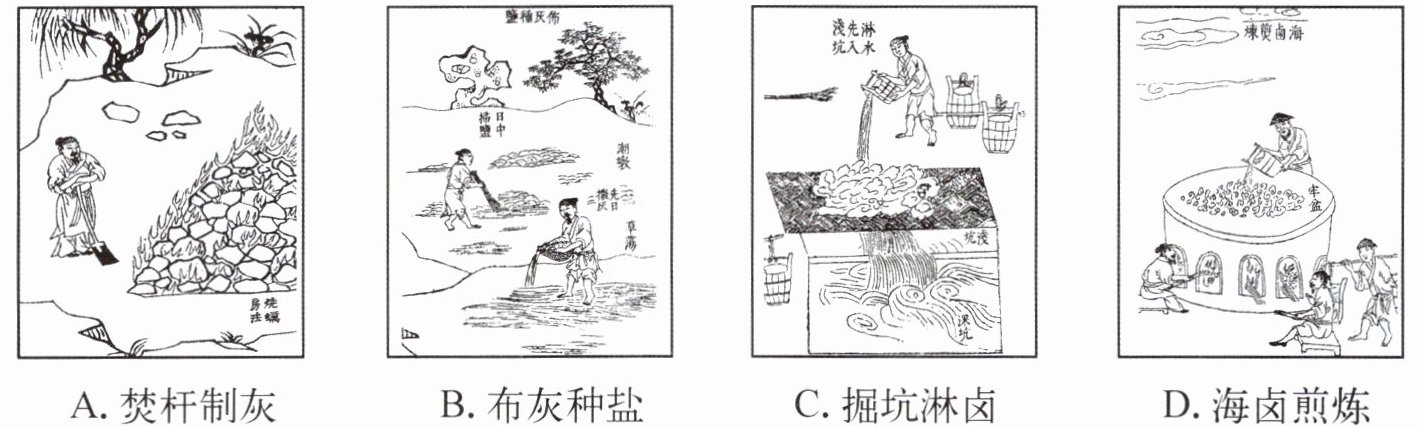
2. 明代《天工开物》记载了古法制盐的过程。下列工序与“蒸发结晶”原理类似的是(
D
)
答案:2 D
解析:
【解析】
A. 焚杆制灰是燃烧植物获取灰烬,属于化学变化,与蒸发结晶无关;
B. 布灰种盐是利用灰的吸附等作用富集盐分,与蒸发结晶原理不同;
C. 掘坑淋卤是通过溶解作用提取灰中的盐分,属于溶解操作,和蒸发结晶无关;
D. 海卤煎炼是通过加热使海卤中的水分蒸发,从而析出盐晶体,该过程与蒸发结晶原理相同,都是通过蒸发溶剂得到溶质晶体。
【答案】
D
【知识点】
蒸发结晶,物质分离
【点评】
本题以明代《天工开物》中的古法制盐工序为载体,将化学原理与传统文化相融合,考查学生对蒸发结晶原理的理解,引导学生关注化学在传统工艺中的应用。
【难度系数】
0.6
A. 焚杆制灰是燃烧植物获取灰烬,属于化学变化,与蒸发结晶无关;
B. 布灰种盐是利用灰的吸附等作用富集盐分,与蒸发结晶原理不同;
C. 掘坑淋卤是通过溶解作用提取灰中的盐分,属于溶解操作,和蒸发结晶无关;
D. 海卤煎炼是通过加热使海卤中的水分蒸发,从而析出盐晶体,该过程与蒸发结晶原理相同,都是通过蒸发溶剂得到溶质晶体。
【答案】
D
【知识点】
蒸发结晶,物质分离
【点评】
本题以明代《天工开物》中的古法制盐工序为载体,将化学原理与传统文化相融合,考查学生对蒸发结晶原理的理解,引导学生关注化学在传统工艺中的应用。
【难度系数】
0.6
3. 某混合溶液中含两种固体溶质,可采取降温结晶的方法提纯其中一种含量较多的物质,该方法是利用了两种物质具有不同的(
A.溶解度变化趋势
B.熔点
C.密度
D.式量
A
)A.溶解度变化趋势
B.熔点
C.密度
D.式量
答案:3 A
解析:
【解析】
降温结晶法提纯物质,是利用两种固体溶质的溶解度随温度变化的趋势不同,含量较多的物质溶解度受温度影响较大,降温时会大量结晶析出,从而达到提纯目的,所以该方法利用的是二者溶解度变化趋势的差异。
【答案】
A
【知识点】
降温结晶原理、溶解度变化
【点评】
本题考查结晶提纯方法的原理,需明确不同分离提纯方法所依据的物质性质差异,属于基础概念题,注重对化学分离方法核心原理的理解。
【难度系数】
0.8
降温结晶法提纯物质,是利用两种固体溶质的溶解度随温度变化的趋势不同,含量较多的物质溶解度受温度影响较大,降温时会大量结晶析出,从而达到提纯目的,所以该方法利用的是二者溶解度变化趋势的差异。
【答案】
A
【知识点】
降温结晶原理、溶解度变化
【点评】
本题考查结晶提纯方法的原理,需明确不同分离提纯方法所依据的物质性质差异,属于基础概念题,注重对化学分离方法核心原理的理解。
【难度系数】
0.8
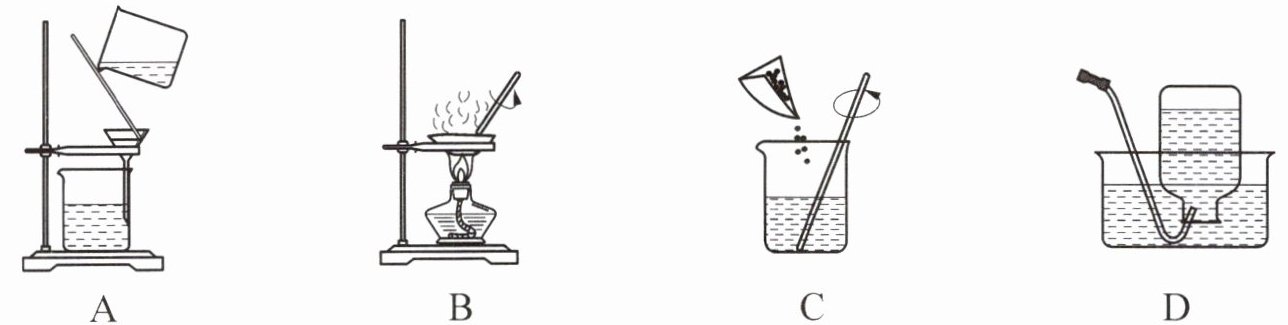
4. 《岭表录异·补遗》记载“野煎盐……则取卤汁,用竹盘煎之,顷刻而就”。这是古人从NaCl溶液中获取NaCl晶体的一种方法,下列实验操作的原理与该描述相符的是(
B
)
答案:4 B
解析:
【解析】
题目描述的是从NaCl溶液中获取NaCl晶体,原理为蒸发结晶。分析各选项:
A为过滤操作,用于分离不溶性固体与液体,与题意不符;
B为蒸发结晶操作,通过加热蒸发溶剂使溶质结晶析出,与题干原理一致;
C为溶解操作,是将固体溶解于溶剂中,与题意不符;
D为排水法收集气体的操作,与题意不符。因此选B。
【答案】
B
【知识点】
蒸发结晶;物质分离操作
【点评】
本题结合古文描述考查化学实验基本操作,需准确理解各操作的原理与适用场景,提升知识迁移应用能力。
【难度系数】
0.7
题目描述的是从NaCl溶液中获取NaCl晶体,原理为蒸发结晶。分析各选项:
A为过滤操作,用于分离不溶性固体与液体,与题意不符;
B为蒸发结晶操作,通过加热蒸发溶剂使溶质结晶析出,与题干原理一致;
C为溶解操作,是将固体溶解于溶剂中,与题意不符;
D为排水法收集气体的操作,与题意不符。因此选B。
【答案】
B
【知识点】
蒸发结晶;物质分离操作
【点评】
本题结合古文描述考查化学实验基本操作,需准确理解各操作的原理与适用场景,提升知识迁移应用能力。
【难度系数】
0.7
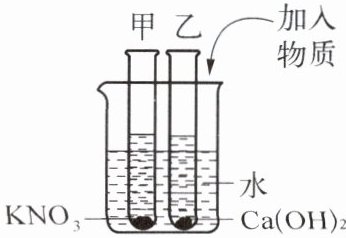
5. 如右图,甲、乙试管中分别盛有硝酸钾、氢氧化钙的饱和溶液,试管底部均有未溶解的固体。向烧杯中加入一定质量的氢氧化钠固体后,下列分析正确的是(
A.甲试管溶液中溶质的质量减小
B.甲试管中溶液的质量减小
C.乙试管中固体的质量增大
D.乙试管溶液中溶质的质量分数增大
C
)
A.甲试管溶液中溶质的质量减小
B.甲试管中溶液的质量减小
C.乙试管中固体的质量增大
D.乙试管溶液中溶质的质量分数增大
答案:解:氢氧化钠固体溶于水放出热量,使溶液温度升高。
硝酸钾的溶解度随温度升高而增大,氢氧化钙的溶解度随温度升高而减小。
- 对于甲试管(硝酸钾饱和溶液):
温度升高,硝酸钾溶解度增大,未溶解的硝酸钾固体继续溶解,所以甲试管中溶质的质量增大,溶液的质量也增大,A、B 错误。
- 对于乙试管(氢氧化钙饱和溶液):
温度升高,氢氧化钙溶解度减小,会有氢氧化钙固体析出,所以乙试管中固体的质量增大,溶质的质量分数减小,C 正确,D 错误。
综上,答案是 C。
硝酸钾的溶解度随温度升高而增大,氢氧化钙的溶解度随温度升高而减小。
- 对于甲试管(硝酸钾饱和溶液):
温度升高,硝酸钾溶解度增大,未溶解的硝酸钾固体继续溶解,所以甲试管中溶质的质量增大,溶液的质量也增大,A、B 错误。
- 对于乙试管(氢氧化钙饱和溶液):
温度升高,氢氧化钙溶解度减小,会有氢氧化钙固体析出,所以乙试管中固体的质量增大,溶质的质量分数减小,C 正确,D 错误。
综上,答案是 C。