1. 不同的物质在同一溶剂中的溶解性不同,如高锰酸钾
可溶
于水,氢氧化钙微溶
于水;同一种物质在不同溶剂中的溶解性不同,如碘
较难溶于水,却易溶于酒精;同一种物质在同一溶剂中的溶解性与温度
有关。答案:1 可溶 微溶 碘 温度
2. 一些固体物质(如
硝酸钾
)在水中的溶解性受温度的影响较大,而对于气体,除温度外,其他因素如压强
也会影响其在水中的溶解。答案:2 硝酸钾 压强
3. 溶解度概念:固体物质的溶解度是指在一定
温度
下,该物质在100
g 溶剂(通常溶剂为水)中达到饱和状态时所溶解的质量。溶解度一般用符号S
表示。答案:3 温度 100 S
1. 下列厨房调料品中,不能溶于水的是(
A.白砂糖
B.辣椒面
C.味精
D.食盐
B
)A.白砂糖
B.辣椒面
C.味精
D.食盐
答案:1 B
解析:
【解析】
白砂糖、味精、食盐均能溶于水形成均一、稳定的溶液;辣椒面的主要成分不溶于水,放入水中会形成悬浊液,因此不能溶于水的是辣椒面。
【答案】
B
【知识点】
物质的溶解性
【点评】
本题考查常见厨房调料品的溶解性,贴近日常生活,需结合生活常识或化学知识进行判断,难度较低。
【难度系数】
0.9
白砂糖、味精、食盐均能溶于水形成均一、稳定的溶液;辣椒面的主要成分不溶于水,放入水中会形成悬浊液,因此不能溶于水的是辣椒面。
【答案】
B
【知识点】
物质的溶解性
【点评】
本题考查常见厨房调料品的溶解性,贴近日常生活,需结合生活常识或化学知识进行判断,难度较低。
【难度系数】
0.9
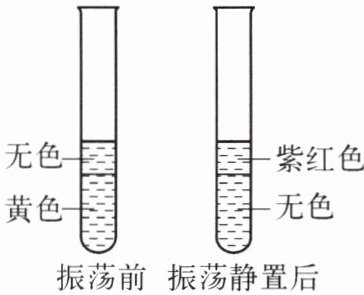
2. 向 6 mL 碘的水溶液(黄色)中加入 2 mL 汽油(无色),振荡静置,实验现象如右图所示。由该实验不能得出的结论是(
A.汽油的密度比水小,且不溶于水
B.碘在汽油中的溶解性比在水中强
C.碘在不同溶剂中形成的溶液颜色可能不同
D.静置后试管中的混合物是溶液
D
)
A.汽油的密度比水小,且不溶于水
B.碘在汽油中的溶解性比在水中强
C.碘在不同溶剂中形成的溶液颜色可能不同
D.静置后试管中的混合物是溶液
答案:2 D
解析:
【解析】
逐一分析各选项:
A. 振荡静置后汽油层在上层,说明汽油密度比水小,且混合物分层,说明汽油不溶于水,该结论可得出;
B. 碘水原本为黄色,静置后下层水层无色,上层汽油层呈紫红色,说明碘更多溶解在汽油中,即碘在汽油中的溶解性比在水中强,该结论可得出;
C. 碘在水中形成黄色溶液,在汽油中形成紫红色溶液,说明碘在不同溶剂中形成的溶液颜色可能不同,该结论可得出;
D. 静置后试管中的混合物分层,不符合溶液均一、稳定的特征,不属于溶液,该结论不能得出。
【答案】
D
【知识点】
溶液的特征、溶解性的影响因素、乳浊液与溶液的区别
【点评】
本题结合碘水与汽油混合的实验现象,考查溶液、溶解性的相关知识,需紧扣实验现象和溶液的基本特征分析选项,注重对实验结论的严谨推导。
【难度系数】
0.6
逐一分析各选项:
A. 振荡静置后汽油层在上层,说明汽油密度比水小,且混合物分层,说明汽油不溶于水,该结论可得出;
B. 碘水原本为黄色,静置后下层水层无色,上层汽油层呈紫红色,说明碘更多溶解在汽油中,即碘在汽油中的溶解性比在水中强,该结论可得出;
C. 碘在水中形成黄色溶液,在汽油中形成紫红色溶液,说明碘在不同溶剂中形成的溶液颜色可能不同,该结论可得出;
D. 静置后试管中的混合物分层,不符合溶液均一、稳定的特征,不属于溶液,该结论不能得出。
【答案】
D
【知识点】
溶液的特征、溶解性的影响因素、乳浊液与溶液的区别
【点评】
本题结合碘水与汽油混合的实验现象,考查溶液、溶解性的相关知识,需紧扣实验现象和溶液的基本特征分析选项,注重对实验结论的严谨推导。
【难度系数】
0.6
3. 已知 20℃时,NaCl 在水中的溶解度为 36 g。下列理解正确的是(
A.20℃时,50 g 水中能够溶解 20 g NaCl
B.20℃时,NaCl 饱和溶液的溶质质量分数为 36%
C.20℃时,36 g NaCl 溶解在 100 g 水中恰好饱和
D.20℃时,NaCl 饱和溶液中溶液与溶质的质量比为 25∶9
C
)A.20℃时,50 g 水中能够溶解 20 g NaCl
B.20℃时,NaCl 饱和溶液的溶质质量分数为 36%
C.20℃时,36 g NaCl 溶解在 100 g 水中恰好饱和
D.20℃时,NaCl 饱和溶液中溶液与溶质的质量比为 25∶9
答案:3 C
解析:
【解析】
根据固体溶解度的定义:在一定温度下,某固态物质在100g溶剂里达到饱和状态时所溶解的质量。20℃时NaCl的溶解度为36g,即20℃时,100g水中溶解36gNaCl恰好达到饱和状态。
A选项:20℃时,50g水中最多溶解NaCl的质量为$36g÷2=18g$,无法溶解20g,故A错误;
B选项:20℃时,NaCl饱和溶液的溶质质量分数为$\frac{36g}{100g+36g}×100\%≈26.5\%$,不是36%,故B错误;
C选项:符合20℃时NaCl溶解度的定义,故C正确;
D选项:20℃时,NaCl饱和溶液中溶液与溶质的质量比为$(100g+36g):36g=34:9$,不是25:9,故D错误。
【答案】
C
【知识点】
固体溶解度概念、溶质质量分数计算
【点评】
本题考查固体溶解度的概念及相关计算,需准确理解溶解度的定义,区分溶解度与溶质质量分数的不同,避免概念混淆。
【难度系数】
0.6
根据固体溶解度的定义:在一定温度下,某固态物质在100g溶剂里达到饱和状态时所溶解的质量。20℃时NaCl的溶解度为36g,即20℃时,100g水中溶解36gNaCl恰好达到饱和状态。
A选项:20℃时,50g水中最多溶解NaCl的质量为$36g÷2=18g$,无法溶解20g,故A错误;
B选项:20℃时,NaCl饱和溶液的溶质质量分数为$\frac{36g}{100g+36g}×100\%≈26.5\%$,不是36%,故B错误;
C选项:符合20℃时NaCl溶解度的定义,故C正确;
D选项:20℃时,NaCl饱和溶液中溶液与溶质的质量比为$(100g+36g):36g=34:9$,不是25:9,故D错误。
【答案】
C
【知识点】
固体溶解度概念、溶质质量分数计算
【点评】
本题考查固体溶解度的概念及相关计算,需准确理解溶解度的定义,区分溶解度与溶质质量分数的不同,避免概念混淆。
【难度系数】
0.6
4. 影响固体物质溶解度的因素有(
① 溶质的多少 ② 溶质的性质 ③ 溶剂的多少 ④ 溶剂的性质 ⑤ 溶液是否饱和 ⑥ 温度
A.②③⑤
B.②④⑥
C.②⑤⑥
D.全部
B
)① 溶质的多少 ② 溶质的性质 ③ 溶剂的多少 ④ 溶剂的性质 ⑤ 溶液是否饱和 ⑥ 温度
A.②③⑤
B.②④⑥
C.②⑤⑥
D.全部
答案:4 B
解析:
【解析】
固体物质的溶解度是指在一定温度下,某固态物质在100g溶剂里达到饱和状态时所溶解的质量。溶解度是物质的固有属性,其大小仅由溶质的性质、溶剂的性质以及温度决定;溶质的多少、溶剂的多少、溶液是否饱和均不会改变物质的溶解度。因此影响固体物质溶解度的因素是②④⑥,故选B。
【答案】
B
【知识点】
固体溶解度影响因素
【点评】
本题考查固体物质溶解度的影响因素,需明确溶解度的定义,区分影响溶解度与影响溶解量的因素,避免混淆无关选项。
【难度系数】
0.7
固体物质的溶解度是指在一定温度下,某固态物质在100g溶剂里达到饱和状态时所溶解的质量。溶解度是物质的固有属性,其大小仅由溶质的性质、溶剂的性质以及温度决定;溶质的多少、溶剂的多少、溶液是否饱和均不会改变物质的溶解度。因此影响固体物质溶解度的因素是②④⑥,故选B。
【答案】
B
【知识点】
固体溶解度影响因素
【点评】
本题考查固体物质溶解度的影响因素,需明确溶解度的定义,区分影响溶解度与影响溶解量的因素,避免混淆无关选项。
【难度系数】
0.7
5. 下列说法正确的是(
A.搅拌可增大物质的溶解度
B.溶液中的溶剂一定是水
C.搅拌和颗粒大小不影响溶解度,仅影响溶解速率
D.自来水厂常在水中加入适量的明矾进行消毒
C
)A.搅拌可增大物质的溶解度
B.溶液中的溶剂一定是水
C.搅拌和颗粒大小不影响溶解度,仅影响溶解速率
D.自来水厂常在水中加入适量的明矾进行消毒
答案:5 C
解析:
【解析】
A选项:溶解度仅与溶质、溶剂的性质和温度有关,搅拌只能加快溶解速率,不能增大物质的溶解度,故A错误;
B选项:溶液中的溶剂不一定是水,例如碘酒中的溶剂是酒精,故B错误;
C选项:溶解度的影响因素为溶质、溶剂的性质和温度,搅拌和颗粒大小不影响溶解度,仅影响溶解速率,故C正确;
D选项:明矾的作用是吸附水中悬浮杂质,加速沉降,不具备消毒功能,故D错误。
【答案】
C
【知识点】
溶解度的影响因素、溶剂的判断、明矾的净水作用
【点评】
本题考查溶液及净水相关基础知识点,重点考查学生对溶解度与溶解速率影响因素的区分,以及常见净水剂功能的掌握,属于基础识记类题目。
【难度系数】
0.8
A选项:溶解度仅与溶质、溶剂的性质和温度有关,搅拌只能加快溶解速率,不能增大物质的溶解度,故A错误;
B选项:溶液中的溶剂不一定是水,例如碘酒中的溶剂是酒精,故B错误;
C选项:溶解度的影响因素为溶质、溶剂的性质和温度,搅拌和颗粒大小不影响溶解度,仅影响溶解速率,故C正确;
D选项:明矾的作用是吸附水中悬浮杂质,加速沉降,不具备消毒功能,故D错误。
【答案】
C
【知识点】
溶解度的影响因素、溶剂的判断、明矾的净水作用
【点评】
本题考查溶液及净水相关基础知识点,重点考查学生对溶解度与溶解速率影响因素的区分,以及常见净水剂功能的掌握,属于基础识记类题目。
【难度系数】
0.8