7. 在餐桌上,当我们发现某种汤太咸时,通常做法是向汤中加入水。在这个过程中,一定改变的是
① 水的质量
② 汤的质量
③ 盐的质量
④ 盐的质量分数
①②④
(填序号,下同),一定不变的是③
。① 水的质量
② 汤的质量
③ 盐的质量
④ 盐的质量分数
答案:7 ①②④ ③
解析:
【解析】
向汤中加入水,水的质量会增加,汤的总质量也会增加;盐的质量未发生改变;盐的质量分数=盐的质量÷汤的总质量,因盐的质量不变、汤的总质量增大,故盐的质量分数减小。因此一定改变的是①②④,一定不变的是③。
【答案】
①②④;③
【知识点】
溶质质量分数计算
【点评】
本题结合生活实例考查溶液相关量的变化,将化学知识与生活场景结合,便于理解溶液中溶质、溶剂、溶液质量及溶质质量分数的变化规律。
【难度系数】
0.8
向汤中加入水,水的质量会增加,汤的总质量也会增加;盐的质量未发生改变;盐的质量分数=盐的质量÷汤的总质量,因盐的质量不变、汤的总质量增大,故盐的质量分数减小。因此一定改变的是①②④,一定不变的是③。
【答案】
①②④;③
【知识点】
溶质质量分数计算
【点评】
本题结合生活实例考查溶液相关量的变化,将化学知识与生活场景结合,便于理解溶液中溶质、溶剂、溶液质量及溶质质量分数的变化规律。
【难度系数】
0.8
8. 将质量分数为 10%的食盐水倒掉一半,余下的食盐水的质量分数为
10%
。一瓶硝酸钾溶液,上层的质量分数为 12%,则下层的质量分数为12%
。将 70℃时 15%的硫酸铜溶液降温至 20℃(无晶体析出),此时硫酸铜溶液的质量分数为15%
。答案:8 10% 12% 15%
解析:
10\%;12\%;15\%
9. 海水淡化可采用膜分离技术。如右图所示,对淡化膜右侧的海水加压,水分子可透过淡化膜进入左侧淡水池,而海水中各种离子不能透过淡化膜,从而得到淡水。加压后,右侧海水中发生变化的量有
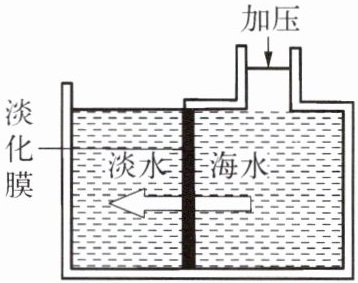
A.溶质质量
B.溶剂质量
C.溶液质量
D.溶质质量分数
BCD
(填字母)。
A.溶质质量
B.溶剂质量
C.溶液质量
D.溶质质量分数
答案:9 BCD
解析:
【解析】
对淡化膜右侧的海水加压后,海水中的水分子可透过淡化膜进入左侧,而海水中的各种离子不能透过淡化膜:
1. 溶质为海水中的各种离子,其质量不变,故A不符合;
2. 溶剂为水,部分水分子进入左侧,溶剂质量减少,故B符合;
3. 溶液质量=溶质质量+溶剂质量,溶剂质量减少,因此溶液质量减少,故C符合;
4. 溶质质量分数=$\frac{溶质质量}{溶液质量}$,溶质质量不变,溶液质量减少,所以溶质质量分数增大,故D符合。
综上,选BCD。
【答案】
BCD
【知识点】
溶液的组成、溶质质量分数计算
【点评】
本题结合膜分离技术考查溶液相关知识,需明确溶质、溶剂、溶液的质量变化关系,理解物质透过性对溶液各成分的影响,体现化学知识在实际生产中的应用。
【难度系数】
0.6
对淡化膜右侧的海水加压后,海水中的水分子可透过淡化膜进入左侧,而海水中的各种离子不能透过淡化膜:
1. 溶质为海水中的各种离子,其质量不变,故A不符合;
2. 溶剂为水,部分水分子进入左侧,溶剂质量减少,故B符合;
3. 溶液质量=溶质质量+溶剂质量,溶剂质量减少,因此溶液质量减少,故C符合;
4. 溶质质量分数=$\frac{溶质质量}{溶液质量}$,溶质质量不变,溶液质量减少,所以溶质质量分数增大,故D符合。
综上,选BCD。
【答案】
BCD
【知识点】
溶液的组成、溶质质量分数计算
【点评】
本题结合膜分离技术考查溶液相关知识,需明确溶质、溶剂、溶液的质量变化关系,理解物质透过性对溶液各成分的影响,体现化学知识在实际生产中的应用。
【难度系数】
0.6
10. 溶液的配制是日常生活和化学实验中的常见操作。硫酸溶液和氨水的密度与其溶质质量分数对照表如下(20℃)。
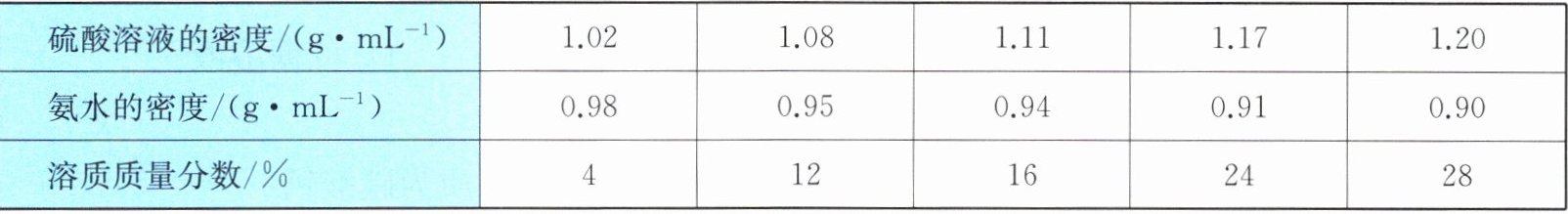
回答下列问题:
(1)20℃时,随着溶液中溶质质量分数逐渐增大,氨水的密度逐渐
(2)将 100 mL 溶质质量分数为 16%的硫酸与 100 mL 水混匀后,所得溶液的溶质质量分数

回答下列问题:
(1)20℃时,随着溶液中溶质质量分数逐渐增大,氨水的密度逐渐
减小
(填“增大”“减小”或“不变”)。(2)将 100 mL 溶质质量分数为 16%的硫酸与 100 mL 水混匀后,所得溶液的溶质质量分数
>
(填“>”“<”或“=”)8%。答案:10 (1) 减小 (2) >
解析:
【解析】
(1) 观察表格中氨水的密度数据,随着溶质质量分数从4%增大到28%,氨水的密度从0.98g·mL⁻¹逐渐减小到0.90g·mL⁻¹,因此20℃时,随着溶液中溶质质量分数逐渐增大,氨水的密度逐渐减小。
(2) 计算过程:
① 100mL溶质质量分数为16%的硫酸溶液质量:$m_{溶液}=ρV=1.11g· mL^{-1}×100mL=111g$
② 溶质硫酸的质量:$m_{溶质}=111g×16\% =17.76g$
③ 加入100mL水后,水的质量为100g,所得溶液总质量:$111g+100g=211g$
④ 所得溶液的溶质质量分数:$\frac{17.76g}{211g}×100\%≈8.42\%$,因此所得溶液的溶质质量分数>8%。
【答案】
(1) 减小
(2) >
【知识点】
溶质质量分数计算、溶液密度与浓度关系
【点评】
本题结合表格数据,考查对溶液密度与溶质质量分数关系的分析,以及溶质质量分数的计算,需灵活运用数据和公式进行判断。
【难度系数】
0.6
(1) 观察表格中氨水的密度数据,随着溶质质量分数从4%增大到28%,氨水的密度从0.98g·mL⁻¹逐渐减小到0.90g·mL⁻¹,因此20℃时,随着溶液中溶质质量分数逐渐增大,氨水的密度逐渐减小。
(2) 计算过程:
① 100mL溶质质量分数为16%的硫酸溶液质量:$m_{溶液}=ρV=1.11g· mL^{-1}×100mL=111g$
② 溶质硫酸的质量:$m_{溶质}=111g×16\% =17.76g$
③ 加入100mL水后,水的质量为100g,所得溶液总质量:$111g+100g=211g$
④ 所得溶液的溶质质量分数:$\frac{17.76g}{211g}×100\%≈8.42\%$,因此所得溶液的溶质质量分数>8%。
【答案】
(1) 减小
(2) >
【知识点】
溶质质量分数计算、溶液密度与浓度关系
【点评】
本题结合表格数据,考查对溶液密度与溶质质量分数关系的分析,以及溶质质量分数的计算,需灵活运用数据和公式进行判断。
【难度系数】
0.6
11. 两个同学在家中做了如下图所示实验:在 A、B、C、D 四个烧杯的水中加入食盐(每勺食盐质量均为 5 g),待食盐完全溶解后,所得溶液中溶质质量分数相等的是
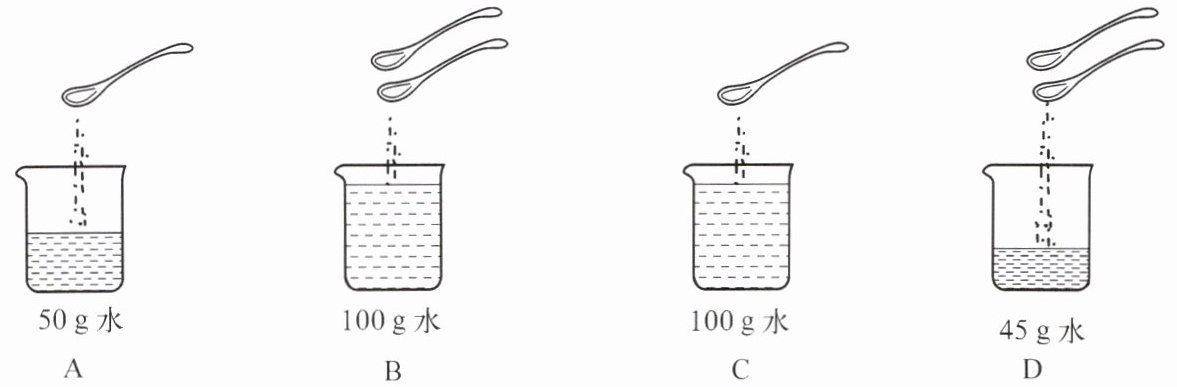
A、B
(填字母,下同),溶质质量分数之比为 2∶1 的是D、A(或 D、B)
。完全溶解后,烧杯中溶质质量分数最大的是D
。
答案:11 A、B D、A(或 D、B) D [解析] 根据溶质质量分数=$\frac{溶质质量}{溶液质量}$×100%,可得,A烧杯中,溶质质量分数=$\frac{5g}{50g+5g}$×100%≈9.1%;B烧杯中,溶质质量分数=$\frac{10g}{100g+10g}$×100%≈9.1%;C烧杯中,溶质质量分数=$\frac{5g}{100g+5g}$×100%≈4.8%;D烧杯中,溶质质量分数=$\frac{10g}{45g+10g}$×100%≈18.2%。由以上数据可知,溶质质量分数相等的是 A、B烧杯,溶质质量分数之比为 2:1 的是 D烧杯与 A(或 B)烧杯,烧杯中溶质质量分数最大的是 D。
解析:
A、B;D、A(或 D、B);D