11. 某同学设计如图甲所示实验,研究KNO₃的溶解度随温度的变化。当向试管中加入一定量的水后,锥形瓶中的KNO₃发生如图乙所示的变化。下列说法正确的是(

A.KNO₃的溶解度:甲>乙
B.KNO₃溶液的溶质质量分数:甲<乙
C.乙中的KNO₃溶液一定为该温度下的饱和溶液
D.用硝酸铵代替生石灰也会出现上述现象
B
)
A.KNO₃的溶解度:甲>乙
B.KNO₃溶液的溶质质量分数:甲<乙
C.乙中的KNO₃溶液一定为该温度下的饱和溶液
D.用硝酸铵代替生石灰也会出现上述现象
答案:11.B
解析:
解:
生石灰与水反应放热,使锥形瓶中温度升高,KNO₃溶解度随温度升高而增大,甲中KNO₃晶体溶解,形成乙中溶液。
A. 温度:甲<乙,KNO₃溶解度随温度升高而增大,故溶解度:甲<乙,A错误。
B. 甲为饱和溶液,乙中溶质增多,溶剂质量变化忽略不计,溶质质量分数:甲<乙,B正确。
C. 乙中可能为不饱和溶液,C错误。
D. 硝酸铵溶于水吸热,温度降低,KNO₃溶解度减小,会析出晶体,与现象不符,D错误。
答案:B
生石灰与水反应放热,使锥形瓶中温度升高,KNO₃溶解度随温度升高而增大,甲中KNO₃晶体溶解,形成乙中溶液。
A. 温度:甲<乙,KNO₃溶解度随温度升高而增大,故溶解度:甲<乙,A错误。
B. 甲为饱和溶液,乙中溶质增多,溶剂质量变化忽略不计,溶质质量分数:甲<乙,B正确。
C. 乙中可能为不饱和溶液,C错误。
D. 硝酸铵溶于水吸热,温度降低,KNO₃溶解度减小,会析出晶体,与现象不符,D错误。
答案:B
12. 25℃时,4种洗手液的pH如下图所示。下列说法中错误的是(
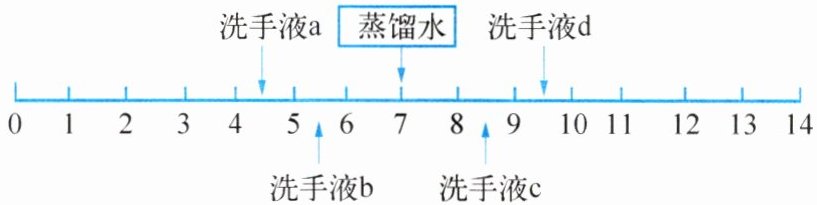
A.a的酸性比b的强
B.a用蒸馏水稀释后pH减小
C.c的碱性比d的弱
D.a和d混合液的pH可能等于7
B
)
A.a的酸性比b的强
B.a用蒸馏水稀释后pH减小
C.c的碱性比d的弱
D.a和d混合液的pH可能等于7
答案:12.B
解析:
A. a的pH=4,b的pH=5,pH越小酸性越强,a的酸性比b的强,正确。
B. a显酸性,用蒸馏水稀释后酸性减弱,pH增大,错误。
C. c的pH=8,d的pH=9,pH越大碱性越强,c的碱性比d的弱,正确。
D. a显酸性,d显碱性,混合后pH可能等于7,正确。
答案:B
B. a显酸性,用蒸馏水稀释后酸性减弱,pH增大,错误。
C. c的pH=8,d的pH=9,pH越大碱性越强,c的碱性比d的弱,正确。
D. a显酸性,d显碱性,混合后pH可能等于7,正确。
答案:B
13. 盐水洗鼻法是防治感冒的手段之一,某同学用50.0g水配制0.9%的洗鼻液(NaCl溶液),以下关于该溶液配制的说法正确的是(
A.溶解时玻璃棒的作用是加快溶解
B.用250mL量筒量取50mL水
C.需称取NaCl的质量为4.5g
D.装瓶时溶液洒落会导致浓度偏低
A
)A.溶解时玻璃棒的作用是加快溶解
B.用250mL量筒量取50mL水
C.需称取NaCl的质量为4.5g
D.装瓶时溶液洒落会导致浓度偏低
答案:13.A
14. 为探究稀盐酸和氢氧化钠溶液反应过程中溶液的pH及温度随时间的变化关系,右图是数字采集器和计算机实时显示的数据曲线。下列说法错误的是(
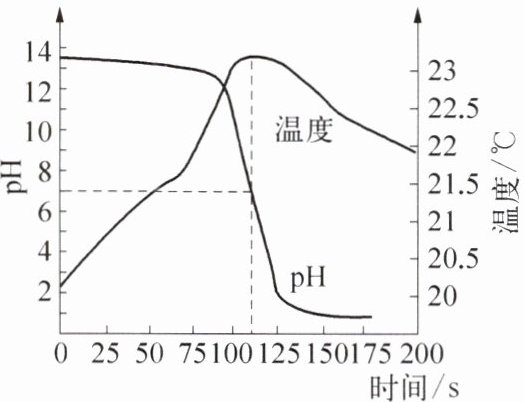
A.实验开始时,烧杯中盛有的试剂是氢氧化钠溶液
B.0~100s时,温度上升是因为该反应放热
C.100s时,溶液中Na⁺和Cl⁻的个数比等于1:1
D.反应本质是H⁺与OH⁻作用生成H₂O
C
)
A.实验开始时,烧杯中盛有的试剂是氢氧化钠溶液
B.0~100s时,温度上升是因为该反应放热
C.100s时,溶液中Na⁺和Cl⁻的个数比等于1:1
D.反应本质是H⁺与OH⁻作用生成H₂O
答案:14.C
15. 科学家研究开发氢能源的脚步从未停止,下图为我国科学家研发的制取和贮存氢气的新工艺。下列有关说法正确的是(

A.图中共有四种氧化物
B.循环制氢反应中需要不断加入ZnFe₂O₄
C.与传统电解法制取氢气相比,该工艺的优点是节约能源
D.反应3中通入氩气作保护气,是利用氩气的化学性质比较活泼
C
)
A.图中共有四种氧化物
B.循环制氢反应中需要不断加入ZnFe₂O₄
C.与传统电解法制取氢气相比,该工艺的优点是节约能源
D.反应3中通入氩气作保护气,是利用氩气的化学性质比较活泼
答案:15.C