7. 溶质质量分数为 16%的氯化钠溶液可用于农业选种。配制 100g 溶质质量分数为 16%的氯化钠溶液,需要氯化钠的质量为
16
g,溶解时用到的玻璃仪器有烧杯(或玻璃棒)
(任写一种),往烧杯中加入量好的水时有水洒出,这样会导致所配溶液的溶质质量分数(其他操作均正确)偏大
(填“偏大”“偏小”或“不变”)。答案:7. 16 烧杯(或玻璃棒) 偏大
解析:
【解析】
1. 计算所需氯化钠质量:根据溶质质量=溶液质量×溶质质量分数,可得氯化钠质量为100g×16%=16g;
2. 溶解时用到的玻璃仪器有烧杯、玻璃棒等,任写一种即可;
3. 往烧杯中加入量好的水时有水洒出,会导致实际溶剂质量偏小,溶质质量不变,根据溶质质量分数公式,所配溶液的溶质质量分数偏大。
【答案】
16;烧杯(或玻璃棒);偏大
【知识点】
溶液配制;溶质质量分数计算;误差分析
【点评】
本题考查溶液配制的计算、操作仪器及误差分析,属于基础题型,聚焦溶液配制的核心考点。
【难度系数】
0.8
1. 计算所需氯化钠质量:根据溶质质量=溶液质量×溶质质量分数,可得氯化钠质量为100g×16%=16g;
2. 溶解时用到的玻璃仪器有烧杯、玻璃棒等,任写一种即可;
3. 往烧杯中加入量好的水时有水洒出,会导致实际溶剂质量偏小,溶质质量不变,根据溶质质量分数公式,所配溶液的溶质质量分数偏大。
【答案】
16;烧杯(或玻璃棒);偏大
【知识点】
溶液配制;溶质质量分数计算;误差分析
【点评】
本题考查溶液配制的计算、操作仪器及误差分析,属于基础题型,聚焦溶液配制的核心考点。
【难度系数】
0.8
8. 某葡萄糖(C₆H₁₂O₆)注射液的标签如右表所示。
(1)葡萄糖中碳元素的质量分数为
(2)要把 10g 这种葡萄糖溶液稀释为溶质质量分数为 2%的溶液,稀释所需水的质量为
(1)葡萄糖中碳元素的质量分数为
40
%。(2)要把 10g 这种葡萄糖溶液稀释为溶质质量分数为 2%的溶液,稀释所需水的质量为
15
g。答案:8. (1)40 (2)15
解析:
【解析】
(1)葡萄糖中碳元素的质量分数为:$\frac{12×6}{12×6+1×12+16×6}×100\%=\frac{72}{180}×100\%=40\%$。
(2)10g该葡萄糖溶液中溶质的质量为$10g×5\%=0.5g$(原溶液溶质质量分数为5%);稀释前后溶质质量不变,设稀释后溶液质量为$x$,则$2\%x=0.5g$,解得$x=25g$;所需水的质量为$25g-10g=15g$。
【答案】
(1)40 (2)15
【知识点】
元素质量分数计算;溶液的稀释计算
【点评】
本题考查化学式计算与溶液稀释的基础运算,需掌握元素质量分数公式及溶液稀释前后溶质质量守恒的核心原理。
【难度系数】
0.7
(1)葡萄糖中碳元素的质量分数为:$\frac{12×6}{12×6+1×12+16×6}×100\%=\frac{72}{180}×100\%=40\%$。
(2)10g该葡萄糖溶液中溶质的质量为$10g×5\%=0.5g$(原溶液溶质质量分数为5%);稀释前后溶质质量不变,设稀释后溶液质量为$x$,则$2\%x=0.5g$,解得$x=25g$;所需水的质量为$25g-10g=15g$。
【答案】
(1)40 (2)15
【知识点】
元素质量分数计算;溶液的稀释计算
【点评】
本题考查化学式计算与溶液稀释的基础运算,需掌握元素质量分数公式及溶液稀释前后溶质质量守恒的核心原理。
【难度系数】
0.7
9. 配制一定溶质质量分数的氯化钠溶液的过程如图 1 所示。
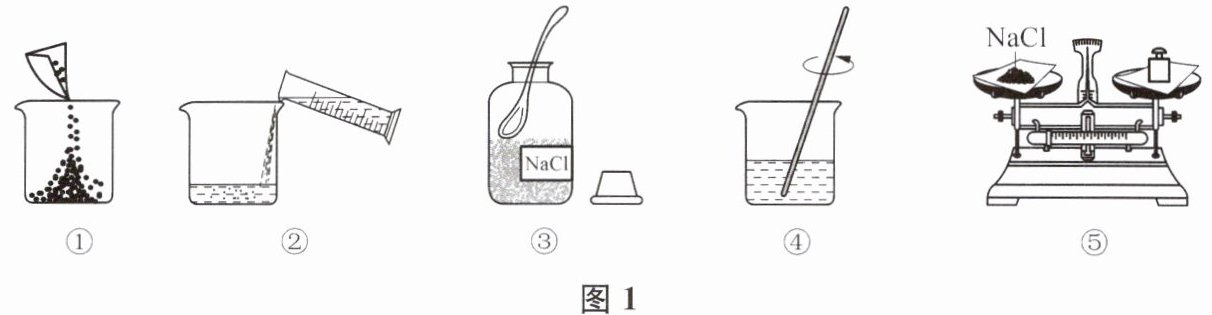
(1)写出图 1 中标号⑤仪器的名称:
(2)上述实验操作顺序为
(3)下列操作可能导致溶质质量分数偏小的是
A. 称量时,药品与砝码位置放反了(使用游码)
B. 烧杯水洗后直接配制溶液
C. 装瓶时,有少量溶液洒出
D. 量取水的体积时,俯视读数
(4)根据图 2、图 3 可知,该小组同学配制的 NaCl 溶液溶质质量分数为
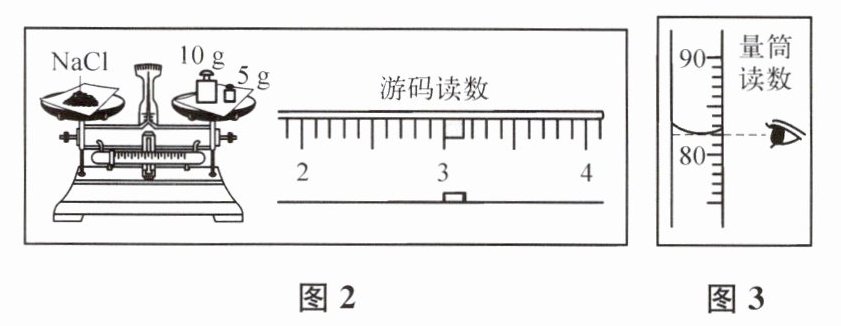
(5)装瓶贴签:标签中应标出

(1)写出图 1 中标号⑤仪器的名称:
托盘天平
。(2)上述实验操作顺序为
③⑤①②④
(填序号)。(3)下列操作可能导致溶质质量分数偏小的是
AB
(填字母)。A. 称量时,药品与砝码位置放反了(使用游码)
B. 烧杯水洗后直接配制溶液
C. 装瓶时,有少量溶液洒出
D. 量取水的体积时,俯视读数
(4)根据图 2、图 3 可知,该小组同学配制的 NaCl 溶液溶质质量分数为
18%
。
(5)装瓶贴签:标签中应标出
溶液的名称
和溶液中溶质的质量分数。答案:9. (1)托盘天平 (2)③⑤①②④ (3)AB (4)18% (5)溶液的名称
解析:
【解析】
(1) 标号⑤的仪器是用于称量固体药品质量的托盘天平。
(2) 配制一定溶质质量分数溶液的步骤为计算、称量、量取、溶解、装瓶贴签,对应图中操作顺序为③⑤①②④。
(3) A. 称量时药品与砝码放反且使用游码,会导致称量的溶质质量偏小,溶质质量分数偏小;B. 烧杯水洗后直接配制,会使溶剂质量偏大,溶质质量分数偏小;C. 装瓶时溶液洒出,溶液具有均一性,溶质质量分数不变;D. 俯视量取水,量取的水体积偏小,溶质质量分数偏大,故选AB。
(4) 由图2可知,称量的NaCl质量为15g+3g=18g;由图3可知,量取水的体积为82mL,水的质量为82g,溶液总质量为18g+82g=100g,溶质质量分数为$\frac{18g}{100g}×100\%=18\%$。
(5) 装瓶贴签时,标签应标注溶液的名称和溶质的质量分数。
【答案】
(1) 托盘天平
(2) ③⑤①②④
(3) AB
(4) 18%
(5) 溶液的名称
【知识点】
一定溶质质量分数的溶液配制、溶质质量分数误差分析、实验仪器识别
【点评】
本题围绕配制一定溶质质量分数的氯化钠溶液展开,考查了实验仪器识别、操作顺序、误差分析、溶质质量分数计算及标签填写,涵盖了溶液配制实验的核心知识点,注重对实验基本技能和原理的考查,属于基础型实验题。
【难度系数】
0.7
(1) 标号⑤的仪器是用于称量固体药品质量的托盘天平。
(2) 配制一定溶质质量分数溶液的步骤为计算、称量、量取、溶解、装瓶贴签,对应图中操作顺序为③⑤①②④。
(3) A. 称量时药品与砝码放反且使用游码,会导致称量的溶质质量偏小,溶质质量分数偏小;B. 烧杯水洗后直接配制,会使溶剂质量偏大,溶质质量分数偏小;C. 装瓶时溶液洒出,溶液具有均一性,溶质质量分数不变;D. 俯视量取水,量取的水体积偏小,溶质质量分数偏大,故选AB。
(4) 由图2可知,称量的NaCl质量为15g+3g=18g;由图3可知,量取水的体积为82mL,水的质量为82g,溶液总质量为18g+82g=100g,溶质质量分数为$\frac{18g}{100g}×100\%=18\%$。
(5) 装瓶贴签时,标签应标注溶液的名称和溶质的质量分数。
【答案】
(1) 托盘天平
(2) ③⑤①②④
(3) AB
(4) 18%
(5) 溶液的名称
【知识点】
一定溶质质量分数的溶液配制、溶质质量分数误差分析、实验仪器识别
【点评】
本题围绕配制一定溶质质量分数的氯化钠溶液展开,考查了实验仪器识别、操作顺序、误差分析、溶质质量分数计算及标签填写,涵盖了溶液配制实验的核心知识点,注重对实验基本技能和原理的考查,属于基础型实验题。
【难度系数】
0.7
10. 请将下列实验报告补充完整。

② 称量:用托盘天平称量所需的氯化钠,放入烧杯中。
③ 量取:用量筒量取所需的水(水的密度可近似看作 1g·mL⁻¹),倒入盛有氯化钠的烧杯中。

② 称量:用托盘天平称量所需的氯化钠,放入烧杯中。
③ 量取:用量筒量取所需的水(水的密度可近似看作 1g·mL⁻¹),倒入盛有氯化钠的烧杯中。
答案:10. 3 47 减少氯化钠的质量,直至天平平衡 大 搅拌,加快溶解速率
解析:
【解析】
1. 计算:溶质质量=溶液质量×溶质质量分数,故氯化钠质量为$50\ \mathrm{g} × 6\% = 3\ \mathrm{g}$,水的质量为$50\ \mathrm{g} - 3\ \mathrm{g} = 47\ \mathrm{g}$。
2. 天平使用:天平左侧下沉,说明左盘氯化钠质量偏大,接下来应减少氯化钠的质量,直至天平平衡。
3. 量筒读数误差:俯视读数时,量取的水的实际体积偏小,水的质量偏小,根据溶质质量分数公式,会导致溶质质量分数偏大。
4. 玻璃棒作用:溶解时用玻璃棒搅拌,目的是加快溶解速率。
【答案】
3;47;减少氯化钠的质量,直至天平平衡;大;搅拌,加快溶解速率
【知识点】
1. 一定溶质质量分数溶液的配制
2. 托盘天平的使用
3. 量筒读数误差分析
【点评】
本题围绕氯化钠溶液的配制展开,考查了溶液配制的计算、天平与量筒的操作要点及误差分析,属于基础实验题,注重对实验基本操作和原理的考查,是中考化学实验部分的常考内容。
【难度系数】
0.8
1. 计算:溶质质量=溶液质量×溶质质量分数,故氯化钠质量为$50\ \mathrm{g} × 6\% = 3\ \mathrm{g}$,水的质量为$50\ \mathrm{g} - 3\ \mathrm{g} = 47\ \mathrm{g}$。
2. 天平使用:天平左侧下沉,说明左盘氯化钠质量偏大,接下来应减少氯化钠的质量,直至天平平衡。
3. 量筒读数误差:俯视读数时,量取的水的实际体积偏小,水的质量偏小,根据溶质质量分数公式,会导致溶质质量分数偏大。
4. 玻璃棒作用:溶解时用玻璃棒搅拌,目的是加快溶解速率。
【答案】
3;47;减少氯化钠的质量,直至天平平衡;大;搅拌,加快溶解速率
【知识点】
1. 一定溶质质量分数溶液的配制
2. 托盘天平的使用
3. 量筒读数误差分析
【点评】
本题围绕氯化钠溶液的配制展开,考查了溶液配制的计算、天平与量筒的操作要点及误差分析,属于基础实验题,注重对实验基本操作和原理的考查,是中考化学实验部分的常考内容。
【难度系数】
0.8