1.下列关于化学方程式S十O2点燃SO2提供的信息,正确的是 (
A.硫加氧气等于二氧化硫
B.硫元素和氧元素反应生成二氧化硫
C.硫和氧气在点燃的条件下反应生成二氧化硫
D.每32份质量的硫与16份质量的氧气恰好完全反应生成48份质量的二氧化硫
C
)A.硫加氧气等于二氧化硫
B.硫元素和氧元素反应生成二氧化硫
C.硫和氧气在点燃的条件下反应生成二氧化硫
D.每32份质量的硫与16份质量的氧气恰好完全反应生成48份质量的二氧化硫
答案:C
2.化学反应前后肯定没有变化的是 (
①原子数目 ②分子数目 ③元素种类 ④物质种类 5原子种类 ⑥物质的总质量
A.①④⑥
B.②③⑤
C.①②⑥
D.①③⑤⑥
D
) ①原子数目 ②分子数目 ③元素种类 ④物质种类 5原子种类 ⑥物质的总质量
A.①④⑥
B.②③⑤
C.①②⑥
D.①③⑤⑥
答案:D
解析:
根据质量守恒定律,化学反应前后原子数目、原子种类、元素种类及物质的总质量均不变;分子数目可能改变,物质种类一定改变。因此肯定没有变化的是①③⑤⑥。
答案:D
答案:D
3.航天员在空间站内呼吸产生的二氧化碳和水可以通过以下反应除去:4X+4CO2+2H2O-
4KHCO3+3O2,则X的化学式为 (
A.K2O
B.KOH
C.K2O2
D.KO2
4KHCO3+3O2,则X的化学式为 (
D
)A.K2O
B.KOH
C.K2O2
D.KO2
答案:D
解析:
解:根据质量守恒定律,化学反应前后原子的种类和数目不变。
反应后:K原子4个,H原子4个,C原子4个,O原子(4×3 + 3×2)= 18个。
反应前:CO₂提供C原子4个、O原子8个;H₂O提供H原子2个、O原子2个。
则4X中含有的原子:K原子4个,H原子(4 - 2)= 2个,O原子(18 - 8 - 2)= 8个。
因此,X中含K原子1个,H原子0.5个(应为整数,此处计算错误,重新分析:反应后H原子总数为4KHCO₃中4个H,反应前H₂O提供2个H,故4X中含H原子4 - 2 = 2个,每个X含H原子0.5个不合理,重新检查:4KHCO₃中H为4×1=4,H₂O中H为2×1=2,反应前H原子总数为2,反应后为4,所以4X中H原子数为4 - 2 = 2,每个X含H原子0.5个,说明之前H计算错误,正确应为反应后H原子4个,反应前H₂O有2个H,所以4X中H原子为4 - 2 = 2,即每个X含H 0.5个,这不可能,说明之前K的计算正确,4X含K 4个,所以X含K 1个;O原子反应后4KHCO₃中O为4×3=12,3O₂中O为6,共18个,反应前CO₂中O为4×2=8,H₂O中O为2,共10个,所以4X中O原子18 - 10 = 8,每个X含O 2个;H原子反应后4个,反应前H₂O有2个,所以4X中H原子2个,每个X含H 0.5个,矛盾,说明化学式中不含H,故H₂O中的H全部在KHCO₃中,4KHCO₃含4个H,H₂O提供2个H,所以4X中H原子为4 - 2 = 2,即X含H 0.5个,错误,应为题目中X不含H,所以反应前H原子只有H₂O的2个,反应后KHCO₃中H为2个,即4KHCO₃应为2KHCO₃,题目中化学方程式为4X + 4CO₂ + 2H₂O = 4KHCO₃ + 3O₂,配平正确的话,KHCO₃中K、H、C、O分别为4、4、4、12,O₂中O为6,共O 18;CO₂中C 4、O 8,H₂O中H 2、O 2,所以4X中含K 4、H 4 - 2 = 2、O 18 - 8 - 2 = 8,即X含K 1、H 0.5、O 2,不合理,故X不含H,H全部来自H₂O,4KHCO₃含4H,H₂O提供2H,所以4X中H为2,不可能,因此原假设错误,正确应为X中不含H,所以H₂O中的H全部进入KHCO₃,4KHCO₃有4H,所以H₂O应为4H₂O,题目中是2H₂O,所以H原子守恒:2×2=4×1,正确,即2H₂O含4H,4KHCO₃含4H,H守恒;K守恒:4X含4K,X含1K;C守恒:4CO₂含4C,4KHCO₃含4C,守恒;O守恒:4X中O + 4CO₂中O(8) + 2H₂O中O(2)= 4KHCO₃中O(12) + 3O₂中O(6),即4X中O + 10 = 18,4X中O=8,X中O=2,所以X为KO₂,不含H,故答案为D。
答案:D
反应后:K原子4个,H原子4个,C原子4个,O原子(4×3 + 3×2)= 18个。
反应前:CO₂提供C原子4个、O原子8个;H₂O提供H原子2个、O原子2个。
则4X中含有的原子:K原子4个,H原子(4 - 2)= 2个,O原子(18 - 8 - 2)= 8个。
因此,X中含K原子1个,H原子0.5个(应为整数,此处计算错误,重新分析:反应后H原子总数为4KHCO₃中4个H,反应前H₂O提供2个H,故4X中含H原子4 - 2 = 2个,每个X含H原子0.5个不合理,重新检查:4KHCO₃中H为4×1=4,H₂O中H为2×1=2,反应前H原子总数为2,反应后为4,所以4X中H原子数为4 - 2 = 2,每个X含H原子0.5个,说明之前H计算错误,正确应为反应后H原子4个,反应前H₂O有2个H,所以4X中H原子为4 - 2 = 2,即每个X含H 0.5个,这不可能,说明之前K的计算正确,4X含K 4个,所以X含K 1个;O原子反应后4KHCO₃中O为4×3=12,3O₂中O为6,共18个,反应前CO₂中O为4×2=8,H₂O中O为2,共10个,所以4X中O原子18 - 10 = 8,每个X含O 2个;H原子反应后4个,反应前H₂O有2个,所以4X中H原子2个,每个X含H 0.5个,矛盾,说明化学式中不含H,故H₂O中的H全部在KHCO₃中,4KHCO₃含4个H,H₂O提供2个H,所以4X中H原子为4 - 2 = 2,即X含H 0.5个,错误,应为题目中X不含H,所以反应前H原子只有H₂O的2个,反应后KHCO₃中H为2个,即4KHCO₃应为2KHCO₃,题目中化学方程式为4X + 4CO₂ + 2H₂O = 4KHCO₃ + 3O₂,配平正确的话,KHCO₃中K、H、C、O分别为4、4、4、12,O₂中O为6,共O 18;CO₂中C 4、O 8,H₂O中H 2、O 2,所以4X中含K 4、H 4 - 2 = 2、O 18 - 8 - 2 = 8,即X含K 1、H 0.5、O 2,不合理,故X不含H,H全部来自H₂O,4KHCO₃含4H,H₂O提供2H,所以4X中H为2,不可能,因此原假设错误,正确应为X中不含H,所以H₂O中的H全部进入KHCO₃,4KHCO₃有4H,所以H₂O应为4H₂O,题目中是2H₂O,所以H原子守恒:2×2=4×1,正确,即2H₂O含4H,4KHCO₃含4H,H守恒;K守恒:4X含4K,X含1K;C守恒:4CO₂含4C,4KHCO₃含4C,守恒;O守恒:4X中O + 4CO₂中O(8) + 2H₂O中O(2)= 4KHCO₃中O(12) + 3O₂中O(6),即4X中O + 10 = 18,4X中O=8,X中O=2,所以X为KO₂,不含H,故答案为D。
答案:D
4.下列关于化学方程式N2+O2高温2NO的说法错误的是 (
A.该反应是化合反应
B.反应中各物质的质量不变
C.遵循质量守恒定律
D.反应前后分子的数目不变
B
)A.该反应是化合反应
B.反应中各物质的质量不变
C.遵循质量守恒定律
D.反应前后分子的数目不变
答案:B
解析:
解:
A. 该反应符合“多变一”的特征,是化合反应,正确。
B. 化学反应遵循质量守恒定律,反应前后总质量不变,但各物质的质量会发生改变,错误。
C. 所有化学反应都遵循质量守恒定律,正确。
D. 反应前分子数目为2(1个N₂分子和1个O₂分子),反应后分子数目为2(2个NO分子),分子数目不变,正确。
结论:错误的是B。
答案:B
A. 该反应符合“多变一”的特征,是化合反应,正确。
B. 化学反应遵循质量守恒定律,反应前后总质量不变,但各物质的质量会发生改变,错误。
C. 所有化学反应都遵循质量守恒定律,正确。
D. 反应前分子数目为2(1个N₂分子和1个O₂分子),反应后分子数目为2(2个NO分子),分子数目不变,正确。
结论:错误的是B。
答案:B
5.四名同学正在讨论某一个化学方程式表示的意义,他们所描述的化学方程式是 (
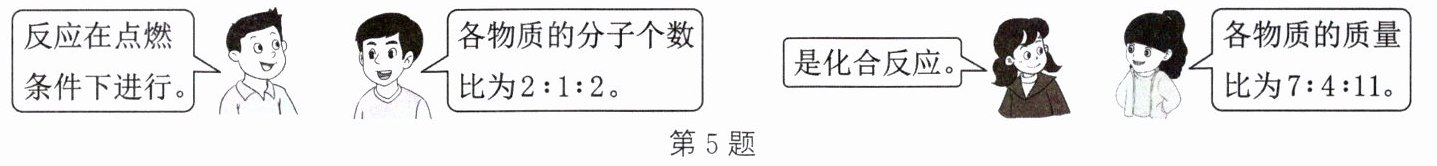
A.CH+2O2点燃CO2+2H20
B.2CO+O2点燃2CO22
C.2H2+O2点燃2H2O
D.H2+C12点燃2HC1
B
)
A.CH+2O2点燃CO2+2H20
B.2CO+O2点燃2CO22
C.2H2+O2点燃2H2O
D.H2+C12点燃2HC1
答案:B
6.写出下列化学方程式中各物质的质量比。(化成最简整数比)
(1)2Mg+O2点燃2MgO:
(2)CO+CuO= Cu+CO2:
(3)CaCO+2HCl= CaCl+H2O+CO2↑:
(1)2Mg+O2点燃2MgO:
$ m(\text{Mg}) : m(\text{O}_2) : m(\text{MgO}) = 3 : 2 : 5 $
(2)CO+CuO= Cu+CO2:
$ m(\text{CO}) : m(\text{CuO}) : m(\text{Cu}) : m(\text{CO}_2) = 7 : 20 : 16 : 11 $
(3)CaCO+2HCl= CaCl+H2O+CO2↑:
$ m(\text{CaCO}_3) : m(\text{HCl}) : m(\text{CaCl}_2) : m(\text{H}_2\text{O}) : m(\text{CO}_2) = 100 : 73 : 111 : 18 : 44 $
。答案:(1) $ m(\text{Mg}) : m(\text{O}_2) : m(\text{MgO}) = 3 : 2 : 5 $ (2) $ m(\text{CO}) : m(\text{CuO}) : m(\text{Cu}) : m(\text{CO}_2) = 7 : 20 : 16 : 11 $ (3) $ m(\text{CaCO}_3) : m(\text{HCl}) : m(\text{CaCl}_2) : m(\text{H}_2\text{O}) : m(\text{CO}_2) = 100 : 73 : 111 : 18 : 44 $
7.质量守恒定律的定量研究对化学科学的发展具有重大意义。
(1)硅(Si)是太阳能电池和电脑芯片中不可缺少的材料。硅生产的过程中有一个重要的化学反应:SiO2+2C意温Si+2X↑。由此推断X的化学式为
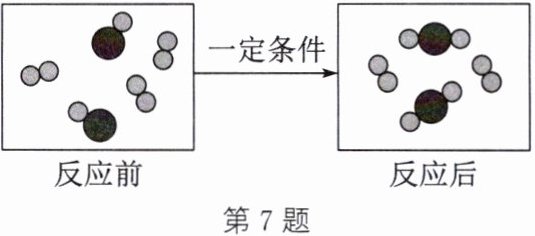
(2)一定条件下,物质A(o)与物质B(∞)反应生成物质C(oo),如图是其反应前后分子变化
的微观示意图(“”和“"表示两种质子数不同的原子)。
①反应前后的原子种类是否发生变化?
 或“否")。
或“否")。
②在A、B、C三种物质中,属于化合物的是
③参与反应的A、B和生成的C的分子个数比为
(1)硅(Si)是太阳能电池和电脑芯片中不可缺少的材料。硅生产的过程中有一个重要的化学反应:SiO2+2C意温Si+2X↑。由此推断X的化学式为
CO
。(2)一定条件下,物质A(o)与物质B(∞)反应生成物质C(oo),如图是其反应前后分子变化
的微观示意图(“”和“"表示两种质子数不同的原子)。
①反应前后的原子种类是否发生变化?
否
(填“是” 或“否")。
或“否")。②在A、B、C三种物质中,属于化合物的是
AC
。③参与反应的A、B和生成的C的分子个数比为
2:1:2
。答案:(1) CO (2) ① 否 ② AC ③ $ 2 : 1 : 2 $