3. 将10 g溶质质量分数为10%氯化钠溶液变为20%,下列操作正确的是(
A.蒸发5 g水
B.加入氯化钠固体1 g
C.倒出一半溶液
D.加入10 g溶质质量分数为10%的氯化钠溶液
A
)A.蒸发5 g水
B.加入氯化钠固体1 g
C.倒出一半溶液
D.加入10 g溶质质量分数为10%的氯化钠溶液
答案:【解析】:
本题考察的是溶液溶质质量分数的计算与理解。
首先,我们需要明确原始溶液的基本信息:10g溶质质量分数为10%的氯化钠溶液,即溶质(氯化钠)的质量为1g,溶剂(水)的质量为9g。
接下来,我们逐一分析每个选项:
A. 蒸发5g水:
如果蒸发5g水,剩余溶液的质量将变为5g(原溶液10g - 蒸发的水5g),但溶质的质量不变,仍为1g。此时,溶质的质量分数为 $\frac{1g}{5g} × 100\% = 20\%$,符合题目要求。
B. 加入氯化钠固体1g:
如果加入1g氯化钠固体,溶质的质量将变为2g(原溶质1g + 新加入的1g),而溶液的质量将变为11g(原溶液10g + 新加入的1g氯化钠固体)。此时,溶质的质量分数为 $\frac{2g}{11g} × 100\% \approx 18.18\%$,不符合题目要求。
C. 倒出一半溶液:
倒出一半溶液后,剩余溶液的质量和溶质的质量都将减半,但溶质的质量分数不变,仍为10%,不符合题目要求。
D. 加入10g溶质质量分数为10%的氯化钠溶液:
加入后,溶液的总质量将变为20g(原溶液10g + 新加入的10g溶液),但溶质的总质量仍为2g(因为新加入的溶液也是10%的氯化钠溶液,所以溶质质量也是1g,加上原溶液的1g)。此时,溶质的质量分数仍为 $\frac{2g}{20g} × 100\% = 10\%$,不符合题目要求。
【答案】:A
本题考察的是溶液溶质质量分数的计算与理解。
首先,我们需要明确原始溶液的基本信息:10g溶质质量分数为10%的氯化钠溶液,即溶质(氯化钠)的质量为1g,溶剂(水)的质量为9g。
接下来,我们逐一分析每个选项:
A. 蒸发5g水:
如果蒸发5g水,剩余溶液的质量将变为5g(原溶液10g - 蒸发的水5g),但溶质的质量不变,仍为1g。此时,溶质的质量分数为 $\frac{1g}{5g} × 100\% = 20\%$,符合题目要求。
B. 加入氯化钠固体1g:
如果加入1g氯化钠固体,溶质的质量将变为2g(原溶质1g + 新加入的1g),而溶液的质量将变为11g(原溶液10g + 新加入的1g氯化钠固体)。此时,溶质的质量分数为 $\frac{2g}{11g} × 100\% \approx 18.18\%$,不符合题目要求。
C. 倒出一半溶液:
倒出一半溶液后,剩余溶液的质量和溶质的质量都将减半,但溶质的质量分数不变,仍为10%,不符合题目要求。
D. 加入10g溶质质量分数为10%的氯化钠溶液:
加入后,溶液的总质量将变为20g(原溶液10g + 新加入的10g溶液),但溶质的总质量仍为2g(因为新加入的溶液也是10%的氯化钠溶液,所以溶质质量也是1g,加上原溶液的1g)。此时,溶质的质量分数仍为 $\frac{2g}{20g} × 100\% = 10\%$,不符合题目要求。
【答案】:A
4. 下面是四位同学在小组学习群中的交流记录,其中错误的是(
A.小云:硝酸铵溶于水后,溶液温度降低
B.小丁:饱和溶液的溶质质量分数不一定大于不饱和溶液的溶质质量分数
C.小丽:具有均一性、稳定性的液体一定是溶液
D.小凯:向饱和溶液中加溶剂可使其变为不饱和溶液
C
)A.小云:硝酸铵溶于水后,溶液温度降低
B.小丁:饱和溶液的溶质质量分数不一定大于不饱和溶液的溶质质量分数
C.小丽:具有均一性、稳定性的液体一定是溶液
D.小凯:向饱和溶液中加溶剂可使其变为不饱和溶液
答案:【解析】:
A. 小云提到硝酸铵溶于水后,溶液温度降低。这是正确的,因为硝酸铵溶于水是一个吸热过程,会使溶液的温度降低。
B. 小丁提到饱和溶液的溶质质量分数不一定大于不饱和溶液的溶质质量分数。这也是正确的,因为溶质质量分数取决于溶质的溶解度和溶液的比例,饱和溶液只是在该温度下不能再溶解更多溶质的溶液,但如果改变温度或溶剂的量,不饱和溶液的溶质质量分数也可能高于饱和溶液。
C. 小丽提到具有均一性、稳定性的液体一定是溶液。这是错误的,因为均一性和稳定性并不能完全确定一个液体是溶液。例如,纯水就具有均一性和稳定性,但它不是溶液。
D. 小凯提到向饱和溶液中加溶剂可使其变为不饱和溶液。这是正确的,因为增加溶剂会降低溶质的浓度,从而使原本饱和的溶液变为不饱和。
【答案】:C
A. 小云提到硝酸铵溶于水后,溶液温度降低。这是正确的,因为硝酸铵溶于水是一个吸热过程,会使溶液的温度降低。
B. 小丁提到饱和溶液的溶质质量分数不一定大于不饱和溶液的溶质质量分数。这也是正确的,因为溶质质量分数取决于溶质的溶解度和溶液的比例,饱和溶液只是在该温度下不能再溶解更多溶质的溶液,但如果改变温度或溶剂的量,不饱和溶液的溶质质量分数也可能高于饱和溶液。
C. 小丽提到具有均一性、稳定性的液体一定是溶液。这是错误的,因为均一性和稳定性并不能完全确定一个液体是溶液。例如,纯水就具有均一性和稳定性,但它不是溶液。
D. 小凯提到向饱和溶液中加溶剂可使其变为不饱和溶液。这是正确的,因为增加溶剂会降低溶质的浓度,从而使原本饱和的溶液变为不饱和。
【答案】:C
5. 溶液在生产、生活中起着十分重要的作用。请回答下列问题:
(1)下列物质属于溶液的是
A. 医用酒精
B. 植物油和水的混合物
C. 蒸馏水
D. 糖水和食盐水的混合物
(2)在配制蔗糖溶液时,蔗糖溶于水并搅拌均匀后,上、下甜度
(3)在木块上滴几滴水,将装有某种固体的大烧杯放置于木块上,向大烧杯中加水并进行搅拌,结果木块上的水结冰了,则大烧杯内的固体可能是
A. 氯化钠
B. 硝酸铵
C. 氢氧化钠
D. 蔗糖
(1)下列物质属于溶液的是
AD
(填字母)。A. 医用酒精
B. 植物油和水的混合物
C. 蒸馏水
D. 糖水和食盐水的混合物
(2)在配制蔗糖溶液时,蔗糖溶于水并搅拌均匀后,上、下甜度
相同
(填“相同”或“不同”),这是因为溶液具有均一
性。(3)在木块上滴几滴水,将装有某种固体的大烧杯放置于木块上,向大烧杯中加水并进行搅拌,结果木块上的水结冰了,则大烧杯内的固体可能是
B
(填字母)。A. 氯化钠
B. 硝酸铵
C. 氢氧化钠
D. 蔗糖
答案:【解析】:
(1)本题考查溶液的定义和特性。溶液是均一、稳定的混合物。
A. 医用酒精是酒精的水溶液,属于溶液;
B. 植物油和水的混合物不均一、不稳定,不属于溶液;
C. 蒸馏水是纯净物,不属于溶液;
D. 糖水和食盐水的混合物,可以看作是糖、盐、水的混合溶液,属于溶液。
故答案选AD。
(2)本题考查溶液的特性。溶液具有均一性,即溶液各部分的性质完全相同。所以蔗糖溶于水并搅拌均匀后,上、下甜度相同。
(3)本题考查物质溶于水时的吸热和放热现象。
A. 氯化钠溶于水时,溶液温度基本不变;
B. 硝酸铵溶于水时,吸收热量,使溶液温度降低;
C. 氢氧化钠溶于水时,放出热量,使溶液温度升高;
D. 蔗糖溶于水时,溶液温度基本不变。
由于木块上的水结冰了,说明大烧杯内的固体溶于水时吸收热量,使溶液温度降低,故可能是硝酸铵。
【答案】:
(1)AD
(2)相同;均一
(3)B
(1)本题考查溶液的定义和特性。溶液是均一、稳定的混合物。
A. 医用酒精是酒精的水溶液,属于溶液;
B. 植物油和水的混合物不均一、不稳定,不属于溶液;
C. 蒸馏水是纯净物,不属于溶液;
D. 糖水和食盐水的混合物,可以看作是糖、盐、水的混合溶液,属于溶液。
故答案选AD。
(2)本题考查溶液的特性。溶液具有均一性,即溶液各部分的性质完全相同。所以蔗糖溶于水并搅拌均匀后,上、下甜度相同。
(3)本题考查物质溶于水时的吸热和放热现象。
A. 氯化钠溶于水时,溶液温度基本不变;
B. 硝酸铵溶于水时,吸收热量,使溶液温度降低;
C. 氢氧化钠溶于水时,放出热量,使溶液温度升高;
D. 蔗糖溶于水时,溶液温度基本不变。
由于木块上的水结冰了,说明大烧杯内的固体溶于水时吸收热量,使溶液温度降低,故可能是硝酸铵。
【答案】:
(1)AD
(2)相同;均一
(3)B
6. 某同学在学习溶液时进行了如图1所示实验探究:
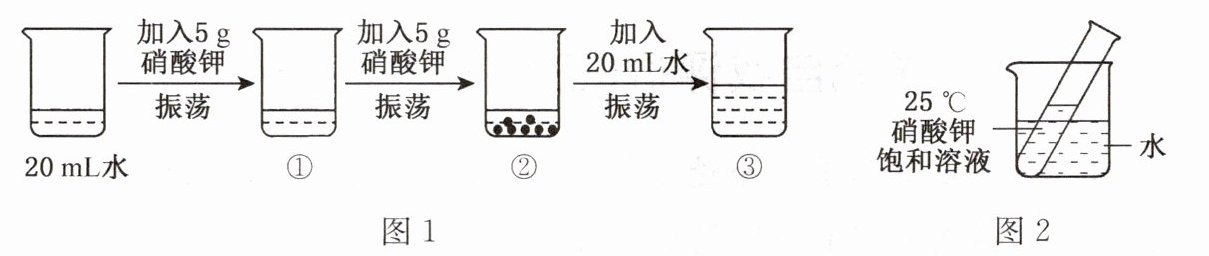 (1)上述①②③烧杯中的溶液,一定属于饱和溶液的是______
(1)上述①②③烧杯中的溶液,一定属于饱和溶液的是______
(2)若要使烧杯②中的剩余固体全部溶解,除了实验中已经采取的措施外,还可以采取的措施为______
(3)如图2所示,若向烧杯中加入足量的硝酸铵固体并使之充分溶解,试管中可观察到的现象是______
 (1)上述①②③烧杯中的溶液,一定属于饱和溶液的是______
(1)上述①②③烧杯中的溶液,一定属于饱和溶液的是______②
(填序号)。(2)若要使烧杯②中的剩余固体全部溶解,除了实验中已经采取的措施外,还可以采取的措施为______
升高温度
。(3)如图2所示,若向烧杯中加入足量的硝酸铵固体并使之充分溶解,试管中可观察到的现象是______
有晶体析出
。答案:【解析】:
(1)饱和溶液是指在一定温度下,一定量的溶剂里不能再溶解某种溶质的溶液。从实验现象可知,②中有剩余固体,说明该温度下,20mL水中不能完全溶解10g硝酸钾,所以②一定是饱和溶液。而①中加入5g硝酸钾后全部溶解,不确定此时是否还能继续溶解硝酸钾,③是在②的基础上又加入了20mL水,固体全部溶解,也不确定是否饱和,所以一定属于饱和溶液的是②。
(2)硝酸钾的溶解度随温度升高而增大,要使烧杯②中的剩余固体全部溶解,除了加水(实验中已采取的措施)外,还可以升高温度。
(3)硝酸铵溶于水吸热,使溶液温度降低,硝酸钾的溶解度随温度降低而减小,所以会有硝酸钾晶体析出,可观察到试管中有晶体析出。
【答案】:
(1)②
(2)升高温度
(3)有晶体析出
(1)饱和溶液是指在一定温度下,一定量的溶剂里不能再溶解某种溶质的溶液。从实验现象可知,②中有剩余固体,说明该温度下,20mL水中不能完全溶解10g硝酸钾,所以②一定是饱和溶液。而①中加入5g硝酸钾后全部溶解,不确定此时是否还能继续溶解硝酸钾,③是在②的基础上又加入了20mL水,固体全部溶解,也不确定是否饱和,所以一定属于饱和溶液的是②。
(2)硝酸钾的溶解度随温度升高而增大,要使烧杯②中的剩余固体全部溶解,除了加水(实验中已采取的措施)外,还可以升高温度。
(3)硝酸铵溶于水吸热,使溶液温度降低,硝酸钾的溶解度随温度降低而减小,所以会有硝酸钾晶体析出,可观察到试管中有晶体析出。
【答案】:
(1)②
(2)升高温度
(3)有晶体析出