9. 化学社团为制作一个可以预测气温变化的简易“天气瓶”,查询到左下图数据。硝酸钾在不同温度时的溶解度如右下表。依据数据,完成下列问题。
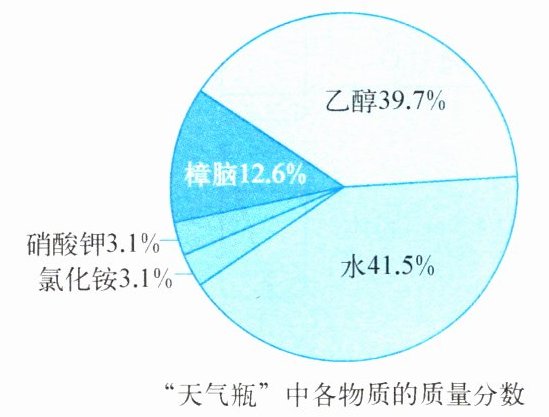

(1) 若“天气瓶”中物质的总质量为 100 g,则含氯化铵的质量是
(2) 计算 10℃时硝酸钾饱和溶液中溶质的质量分数。(列出计算式,结果精确到 0.1%)


(1) 若“天气瓶”中物质的总质量为 100 g,则含氯化铵的质量是
3.1
g。(2) 计算 10℃时硝酸钾饱和溶液中溶质的质量分数。(列出计算式,结果精确到 0.1%)
答案:9 (1)3.1
(2)解:溶质质量分数
$ω=\frac {\mathrm {m}_{溶质}}{\mathrm {m}_{溶液}}×100\%=\frac {\mathrm {m}_{溶质}}{\mathrm {m}_{溶质} + \mathrm {m}_{溶剂}}×100\%。$
由表可知$10°\mathrm {C}$时硝酸钾的溶解度$\mathrm {S} = 20.9\mathrm {g},$
即$10°\mathrm {C}$时,$100\mathrm {g}$水中溶解$20.9\mathrm {g}$硝酸钾达到饱和。
$10°\mathrm {C}$时硝酸钾饱和溶液中溶质的质量分数
$ω=\frac {20.9\mathrm {g}}{20.9\mathrm {g} + 100\mathrm {g}}×100\%≈17.3\%。$
答:$10°\mathrm {C}$时硝酸钾饱和溶液中溶质的质量分数为$17.3\%。$
(2)解:溶质质量分数
$ω=\frac {\mathrm {m}_{溶质}}{\mathrm {m}_{溶液}}×100\%=\frac {\mathrm {m}_{溶质}}{\mathrm {m}_{溶质} + \mathrm {m}_{溶剂}}×100\%。$
由表可知$10°\mathrm {C}$时硝酸钾的溶解度$\mathrm {S} = 20.9\mathrm {g},$
即$10°\mathrm {C}$时,$100\mathrm {g}$水中溶解$20.9\mathrm {g}$硝酸钾达到饱和。
$10°\mathrm {C}$时硝酸钾饱和溶液中溶质的质量分数
$ω=\frac {20.9\mathrm {g}}{20.9\mathrm {g} + 100\mathrm {g}}×100\%≈17.3\%。$
答:$10°\mathrm {C}$时硝酸钾饱和溶液中溶质的质量分数为$17.3\%。$
解析:
【解析】
(1) 由图可知氯化铵的质量分数为$3.1\%$,“天气瓶”中物质总质量为$100g$,根据溶质质量$=$溶液质量$×$溶质质量分数,可得氯化铵质量$=100g×3.1\% = 3.1g$。
(2) 由表格可知$10^{\circ}C$时硝酸钾溶解度为$20.9g$,根据饱和溶液溶质质量分数$=\frac{溶解度}{溶解度 + 100g}×100\%$,则$10^{\circ}C$时硝酸钾饱和溶液溶质质量分数$=\frac{20.9g}{20.9g + 100g}×100\%\approx17.3\%$。
【答案】
(1) $3.1$;
(2)解:溶质质量分数$ω=\frac {\mathrm {m}_{溶质}}{\mathrm {m}_{溶液}}×100\%=\frac {\mathrm {m}_{溶质}}{\mathrm {m}_{溶质} + \mathrm {m}_{溶剂}}×100\%。$
由表可知$10°\mathrm {C}$时硝酸钾的溶解度$\mathrm {S} = 20.9\mathrm {g},$
即$10°\mathrm {C}$时,$100\mathrm {g}$水中溶解$20.9\mathrm {g}$硝酸钾达到饱和。
$10°\mathrm {C}$时硝酸钾饱和溶液中溶质的质量分数
$ω=\frac {20.9\mathrm {g}}{20.9\mathrm {g} + 100\mathrm {g}}×100\%≈17.3\%。$
答:$10°\mathrm {C}$时硝酸钾饱和溶液中溶质的质量分数为$17.3\%。$
【知识点】
溶质质量分数计算、溶解度概念、饱和溶液相关计算
【点评】
本题考查溶液相关计算,第一问根据质量分数计算溶质质量较基础,第二问考查饱和溶液溶质质量分数计算,需准确运用公式。
【难度系数】
$0.6$
(1) 由图可知氯化铵的质量分数为$3.1\%$,“天气瓶”中物质总质量为$100g$,根据溶质质量$=$溶液质量$×$溶质质量分数,可得氯化铵质量$=100g×3.1\% = 3.1g$。
(2) 由表格可知$10^{\circ}C$时硝酸钾溶解度为$20.9g$,根据饱和溶液溶质质量分数$=\frac{溶解度}{溶解度 + 100g}×100\%$,则$10^{\circ}C$时硝酸钾饱和溶液溶质质量分数$=\frac{20.9g}{20.9g + 100g}×100\%\approx17.3\%$。
【答案】
(1) $3.1$;
(2)解:溶质质量分数$ω=\frac {\mathrm {m}_{溶质}}{\mathrm {m}_{溶液}}×100\%=\frac {\mathrm {m}_{溶质}}{\mathrm {m}_{溶质} + \mathrm {m}_{溶剂}}×100\%。$
由表可知$10°\mathrm {C}$时硝酸钾的溶解度$\mathrm {S} = 20.9\mathrm {g},$
即$10°\mathrm {C}$时,$100\mathrm {g}$水中溶解$20.9\mathrm {g}$硝酸钾达到饱和。
$10°\mathrm {C}$时硝酸钾饱和溶液中溶质的质量分数
$ω=\frac {20.9\mathrm {g}}{20.9\mathrm {g} + 100\mathrm {g}}×100\%≈17.3\%。$
答:$10°\mathrm {C}$时硝酸钾饱和溶液中溶质的质量分数为$17.3\%。$
【知识点】
溶质质量分数计算、溶解度概念、饱和溶液相关计算
【点评】
本题考查溶液相关计算,第一问根据质量分数计算溶质质量较基础,第二问考查饱和溶液溶质质量分数计算,需准确运用公式。
【难度系数】
$0.6$
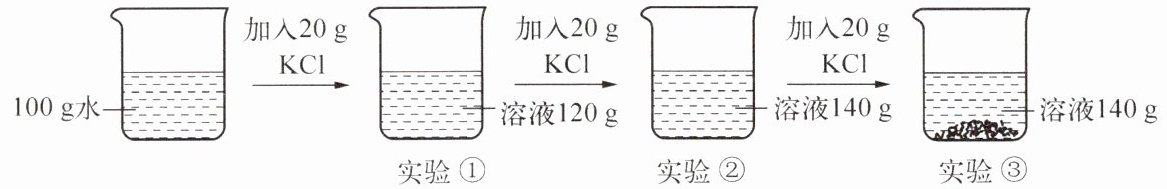
10. 为探究氯化钾的溶解度,进行如下图所示的实验,实验过程中温度不变。
(1) 实验
(2) 该温度下,氯化钾的溶解度为
(3) 三次实验所得溶液溶质质量分数由大到小的顺序是
(4) 给实验③的烧杯中加水,当溶液的质量为

(1) 实验
②③
(填序号)得到的溶液为饱和溶液。(2) 该温度下,氯化钾的溶解度为
40g
。(3) 三次实验所得溶液溶质质量分数由大到小的顺序是
②=③>①
(填序号)。(4) 给实验③的烧杯中加水,当溶液的质量为
210
g 时,氯化钾恰好完全溶解。答案:10 (1)②③ (2)40g (3)②=③>① (4)210
解析:
【解析】
(1) 实验①中100g水加入20gKCl完全溶解,得到120g溶液;实验②中再加入20gKCl,仍完全溶解,得到140g溶液,此时100g水中溶解了40gKCl;实验③中继续加入20gKCl,溶液质量仍为140g,说明该20gKCl未溶解,因此实验②、③得到的溶液为饱和溶液。
(2) 由实验②可知,该温度下100g水中最多能溶解40gKCl,所以此温度下氯化钾的溶解度为40g。
(3) 实验①溶液中溶质质量为20g,实验②、③为该温度下的饱和溶液,溶质质量分数相等,且大于实验①的溶质质量分数,故三次实验所得溶液溶质质量分数由大到小的顺序是②=③>①。
(4) 实验③中有20g未溶解的KCl,设溶解20gKCl需要水的质量为$x$,根据溶解度可得:$\frac{40g}{100g}=\frac{20g}{x}$,解得$x=50g$,则溶液的质量为$140g+50g=210g$。
【答案】
(1) $\boldsymbol{②③}$
(2) $\boldsymbol{40g}$
(3) $\boldsymbol{②=③>①}$
(4) $\boldsymbol{210}$
【知识点】
饱和溶液判断、固体溶解度、溶质质量分数计算
【点评】
本题结合实验探究考查固体溶解度、饱和溶液及溶质质量分数的相关知识,需结合实验现象分析溶液状态,掌握溶解度的计算及溶质质量分数的比较方法。
【难度系数】
0.7
(1) 实验①中100g水加入20gKCl完全溶解,得到120g溶液;实验②中再加入20gKCl,仍完全溶解,得到140g溶液,此时100g水中溶解了40gKCl;实验③中继续加入20gKCl,溶液质量仍为140g,说明该20gKCl未溶解,因此实验②、③得到的溶液为饱和溶液。
(2) 由实验②可知,该温度下100g水中最多能溶解40gKCl,所以此温度下氯化钾的溶解度为40g。
(3) 实验①溶液中溶质质量为20g,实验②、③为该温度下的饱和溶液,溶质质量分数相等,且大于实验①的溶质质量分数,故三次实验所得溶液溶质质量分数由大到小的顺序是②=③>①。
(4) 实验③中有20g未溶解的KCl,设溶解20gKCl需要水的质量为$x$,根据溶解度可得:$\frac{40g}{100g}=\frac{20g}{x}$,解得$x=50g$,则溶液的质量为$140g+50g=210g$。
【答案】
(1) $\boldsymbol{②③}$
(2) $\boldsymbol{40g}$
(3) $\boldsymbol{②=③>①}$
(4) $\boldsymbol{210}$
【知识点】
饱和溶液判断、固体溶解度、溶质质量分数计算
【点评】
本题结合实验探究考查固体溶解度、饱和溶液及溶质质量分数的相关知识,需结合实验现象分析溶液状态,掌握溶解度的计算及溶质质量分数的比较方法。
【难度系数】
0.7
11. 现有四个烧杯分别盛有 50 g 水,在 60℃时,向四个烧杯中分别加入 65 g、60 g、55 g、14 g 硝酸钾,充分溶解后,现象如下图所示。根据 KNO₃的溶解度数据(见下表),回答下列问题。

(1) 20℃时,KNO₃的溶解度为
(2) 烧杯②中溶液的质量是
(3) 下列说法中正确的是
A. 若将四个烧杯中溶液分别升温至 80℃,则烧杯①中溶液的溶质质量分数最大
B. 在 60℃时,上述四个烧杯中溶液的溶质质量分数①=②=③>④
C. 可以利用温度不变向溶液中继续加入原溶质的方法来判断溶液是否饱和
D. 对④中的溶液采用降温的方法可以获得室温(20℃)下的饱和溶液


(1) 20℃时,KNO₃的溶解度为
31.6
g。(2) 烧杯②中溶液的质量是
105
g。(3) 下列说法中正确的是
ABC
(填字母)。A. 若将四个烧杯中溶液分别升温至 80℃,则烧杯①中溶液的溶质质量分数最大
B. 在 60℃时,上述四个烧杯中溶液的溶质质量分数①=②=③>④
C. 可以利用温度不变向溶液中继续加入原溶质的方法来判断溶液是否饱和
D. 对④中的溶液采用降温的方法可以获得室温(20℃)下的饱和溶液
答案:11 (1)31.6 (2)105 (3)ABC
解析:
【解析】
(1) 根据提供的KNO₃溶解度数据,可知20℃时KNO₃的溶解度为31.6g。
(2) 由溶解度表可知,60℃时KNO₃的溶解度为110g,即100g水中最多溶解110g KNO₃,那么50g水中最多溶解55g KNO₃。烧杯②中加入60g KNO₃,充分溶解后只能溶解55g,因此溶液质量为50g + 55g = 105g。
(3) 对各选项分析如下:
A. 80℃时KNO₃的溶解度为169g,50g水中最多能溶解84.5g KNO₃,四个烧杯中加入的硝酸钾质量均小于84.5g,升温至80℃时固体全部溶解,此时烧杯①中溶质质量最大,其溶质质量分数最大,A正确;
B. 60℃时50g水最多溶解55g KNO₃,烧杯①②③中溶解的溶质质量均为55g,溶质质量分数相等;烧杯④中溶解14g KNO₃,溶质质量分数更小,故①=②=③>④,B正确;
C. 温度不变时,向溶液中加入原溶质,若溶质不再溶解则溶液饱和,若能继续溶解则溶液不饱和,该方法可判断溶液是否饱和,C正确;
D. 20℃时50g水最多溶解15.8g KNO₃,烧杯④中溶质仅14g,降温至20℃时溶液仍为不饱和溶液,D错误。
综上,正确选项为ABC。
【答案】
(1) 31.6
(2) 105
(3) ABC
【知识点】
固体溶解度概念,溶质质量分数计算,饱和溶液判断
【点评】
本题围绕硝酸钾的溶解度展开,考查溶解度数据的应用、溶质质量分数计算及饱和溶液的判断等知识点,需结合不同温度下的溶解度分析溶液状态,综合性较强,注重对基础知识的灵活运用。
【难度系数】
0.6
(1) 根据提供的KNO₃溶解度数据,可知20℃时KNO₃的溶解度为31.6g。
(2) 由溶解度表可知,60℃时KNO₃的溶解度为110g,即100g水中最多溶解110g KNO₃,那么50g水中最多溶解55g KNO₃。烧杯②中加入60g KNO₃,充分溶解后只能溶解55g,因此溶液质量为50g + 55g = 105g。
(3) 对各选项分析如下:
A. 80℃时KNO₃的溶解度为169g,50g水中最多能溶解84.5g KNO₃,四个烧杯中加入的硝酸钾质量均小于84.5g,升温至80℃时固体全部溶解,此时烧杯①中溶质质量最大,其溶质质量分数最大,A正确;
B. 60℃时50g水最多溶解55g KNO₃,烧杯①②③中溶解的溶质质量均为55g,溶质质量分数相等;烧杯④中溶解14g KNO₃,溶质质量分数更小,故①=②=③>④,B正确;
C. 温度不变时,向溶液中加入原溶质,若溶质不再溶解则溶液饱和,若能继续溶解则溶液不饱和,该方法可判断溶液是否饱和,C正确;
D. 20℃时50g水最多溶解15.8g KNO₃,烧杯④中溶质仅14g,降温至20℃时溶液仍为不饱和溶液,D错误。
综上,正确选项为ABC。
【答案】
(1) 31.6
(2) 105
(3) ABC
【知识点】
固体溶解度概念,溶质质量分数计算,饱和溶液判断
【点评】
本题围绕硝酸钾的溶解度展开,考查溶解度数据的应用、溶质质量分数计算及饱和溶液的判断等知识点,需结合不同温度下的溶解度分析溶液状态,综合性较强,注重对基础知识的灵活运用。
【难度系数】
0.6