1. 根据$20^{\circ}\mathrm{C}$下物质的溶解度,我们可以将物质分为
易溶
、可溶、微溶
和难溶。答案:1易溶 微溶
2. 溶解度曲线的绘制,以
溶解度
为纵坐标,温度
为横坐标。利用溶解度曲线可以推测物质在不同温度
时的溶解度,可以比较不同物质在相同温度
时溶解度的大小、不同物质的溶解度随温度
变化的趋势。答案:2溶解度 温度 温度 相同温度 温度
1. 工业制备的重铬酸钾(${K2Cr2O7}$)中常混有少量${KCl}$,两种物质的溶解度曲线如右图所示。下列说法正确的是 (
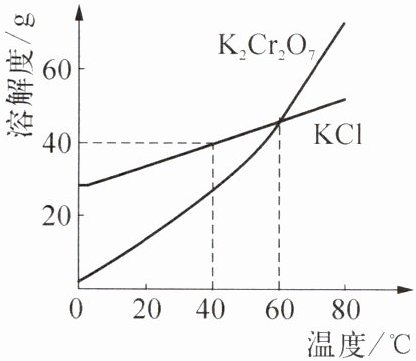
A.${K2Cr2O7}$的溶解度一定比${KCl}$的大
B.$40^{\circ}\mathrm{C}$时,将$50\mathrm{g}{KCl}$加入$100\mathrm{g}$水中,所得溶液质量为$150\mathrm{g}$
C.$60^{\circ}\mathrm{C}$时,两种物质的饱和溶液的溶质质量分数相等
D.采用蒸发结晶的方法可除去${K2Cr2O7}$中混有的少量${KCl}$
C
)
A.${K2Cr2O7}$的溶解度一定比${KCl}$的大
B.$40^{\circ}\mathrm{C}$时,将$50\mathrm{g}{KCl}$加入$100\mathrm{g}$水中,所得溶液质量为$150\mathrm{g}$
C.$60^{\circ}\mathrm{C}$时,两种物质的饱和溶液的溶质质量分数相等
D.采用蒸发结晶的方法可除去${K2Cr2O7}$中混有的少量${KCl}$
答案:1C
解析:
【解析】
- A选项:比较溶解度大小需要指明温度,不指明温度无法比较$K_{2}Cr_{2}O_{7}$与$KCl$溶解度大小,故A错误。
- B选项:由溶解度曲线可知,$40^{\circ}C$时$KCl$的溶解度小于$50g$,将$50gKCl$加入$100g$水中,$KCl$不能完全溶解,所得溶液质量小于$150g$,故B错误。
- C选项:$60^{\circ}C$时,两种物质的溶解度相等,根据饱和溶液溶质质量分数$=\frac{溶解度}{溶解度 + 100g}×100\%$,可知此时两种物质的饱和溶液的溶质质量分数相等,故C正确。
- D选项:$K_{2}Cr_{2}O_{7}$的溶解度受温度影响较大,$KCl$的溶解度受温度影响较小,应采用降温结晶的方法除去$K_{2}Cr_{2}O_{7}$中混有的少量$KCl$,故D错误。
【答案】
C
【知识点】
溶解度曲线、饱和溶液溶质质量分数计算、结晶方法
【点评】
本题考查溶解度曲线相关知识,需要学生理解溶解度曲线的含义,掌握饱和溶液溶质质量分数计算以及结晶方法的选择。
【难度系数】
0.6
- A选项:比较溶解度大小需要指明温度,不指明温度无法比较$K_{2}Cr_{2}O_{7}$与$KCl$溶解度大小,故A错误。
- B选项:由溶解度曲线可知,$40^{\circ}C$时$KCl$的溶解度小于$50g$,将$50gKCl$加入$100g$水中,$KCl$不能完全溶解,所得溶液质量小于$150g$,故B错误。
- C选项:$60^{\circ}C$时,两种物质的溶解度相等,根据饱和溶液溶质质量分数$=\frac{溶解度}{溶解度 + 100g}×100\%$,可知此时两种物质的饱和溶液的溶质质量分数相等,故C正确。
- D选项:$K_{2}Cr_{2}O_{7}$的溶解度受温度影响较大,$KCl$的溶解度受温度影响较小,应采用降温结晶的方法除去$K_{2}Cr_{2}O_{7}$中混有的少量$KCl$,故D错误。
【答案】
C
【知识点】
溶解度曲线、饱和溶液溶质质量分数计算、结晶方法
【点评】
本题考查溶解度曲线相关知识,需要学生理解溶解度曲线的含义,掌握饱和溶液溶质质量分数计算以及结晶方法的选择。
【难度系数】
0.6
2. ${KNO_3}$、${KCl}$可用作钾肥,对大豆的生长具有重要的作用。${KNO_3}$、${KCl}$的溶解度随温度变化的曲线如右图所示,下列说法正确的是 (
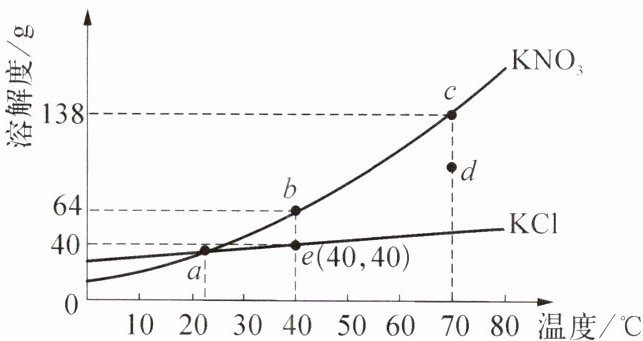
A.$10^{\circ}\mathrm{C}$时,${KNO_3}$和${KCl}$的饱和溶液升温到$22^{\circ}\mathrm{C}$,溶质质量分数不变
B.在$70^{\circ}\mathrm{C}$时,将$238\mathrm{g}{KNO_3}$溶液降温至$40^{\circ}\mathrm{C}$,析出$74\mathrm{g}{KNO_3}$
C.$d$点对应的${KNO_3}$溶液为饱和溶液
D.$e$点对应的${KCl}$饱和溶液中溶质的质量分数为$40\%$
A
)
A.$10^{\circ}\mathrm{C}$时,${KNO_3}$和${KCl}$的饱和溶液升温到$22^{\circ}\mathrm{C}$,溶质质量分数不变
B.在$70^{\circ}\mathrm{C}$时,将$238\mathrm{g}{KNO_3}$溶液降温至$40^{\circ}\mathrm{C}$,析出$74\mathrm{g}{KNO_3}$
C.$d$点对应的${KNO_3}$溶液为饱和溶液
D.$e$点对应的${KCl}$饱和溶液中溶质的质量分数为$40\%$
答案:2A
解析:
【解析】
逐一分析各选项:
A. $10^{\circ}\mathrm{C}$时,${KNO_{3}}$和${KCl}$的饱和溶液升温到$22^{\circ}\mathrm{C}$,二者溶解度均随温度升高而增大,升温后溶液变为不饱和溶液,溶质和溶剂质量均不变,溶质质量分数不变,该选项正确。
B. $70^{\circ}\mathrm{C}$时${KNO_{3}}$溶解度为138g,$40^{\circ}\mathrm{C}$时为64g,但238g${KNO_{3}}$溶液不一定是饱和溶液,降温至$40^{\circ}\mathrm{C}$,析出晶体质量不一定为74g,该选项错误。
C. $d$点在${KNO_{3}}$溶解度曲线的下方,对应的溶液为不饱和溶液,该选项错误。
D. $e$点对应的${KCl}$饱和溶液中,溶质质量分数为$\frac{40\mathrm{g}}{100\mathrm{g}+40\mathrm{g}}×100\%\approx28.6\%$,不是40%,该选项错误。
【答案】
A
【知识点】
溶解度曲线应用;溶质质量分数计算
【点评】
本题考查溶解度曲线的综合应用,需明确溶解度、溶质质量分数的关系,以及饱和溶液与不饱和溶液的转化对溶质质量分数的影响。
【难度系数】
0.7
逐一分析各选项:
A. $10^{\circ}\mathrm{C}$时,${KNO_{3}}$和${KCl}$的饱和溶液升温到$22^{\circ}\mathrm{C}$,二者溶解度均随温度升高而增大,升温后溶液变为不饱和溶液,溶质和溶剂质量均不变,溶质质量分数不变,该选项正确。
B. $70^{\circ}\mathrm{C}$时${KNO_{3}}$溶解度为138g,$40^{\circ}\mathrm{C}$时为64g,但238g${KNO_{3}}$溶液不一定是饱和溶液,降温至$40^{\circ}\mathrm{C}$,析出晶体质量不一定为74g,该选项错误。
C. $d$点在${KNO_{3}}$溶解度曲线的下方,对应的溶液为不饱和溶液,该选项错误。
D. $e$点对应的${KCl}$饱和溶液中,溶质质量分数为$\frac{40\mathrm{g}}{100\mathrm{g}+40\mathrm{g}}×100\%\approx28.6\%$,不是40%,该选项错误。
【答案】
A
【知识点】
溶解度曲线应用;溶质质量分数计算
【点评】
本题考查溶解度曲线的综合应用,需明确溶解度、溶质质量分数的关系,以及饱和溶液与不饱和溶液的转化对溶质质量分数的影响。
【难度系数】
0.7
3. 我国盐湖地区有“夏天晒盐(${NaCl}$),冬天捞碱(${Na_2CO_3}$)”的做法。${NaCl}$、${Na_2CO_3}$的溶解度曲线如右图所示。下列说法正确的是(
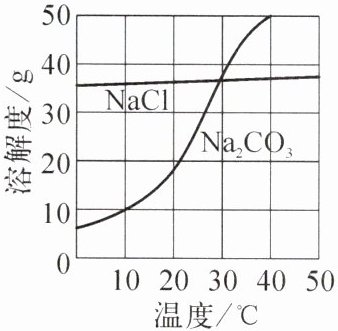
A.$20^{\circ}\mathrm{C}$时,${Na_2CO_3}$的饱和溶液升温到$40^{\circ}\mathrm{C}$仍是饱和溶液
B.$30^{\circ}\mathrm{C}$时,在$100\mathrm{g}$水中加入$40\mathrm{g}{NaCl}$,形成不饱和溶液
C.${NaCl}$的溶解度比${Na_2CO_3}$的大
D.“夏天晒盐”经过蒸发结晶过程,“冬天捞碱”经过降温结晶过程
D
)
A.$20^{\circ}\mathrm{C}$时,${Na_2CO_3}$的饱和溶液升温到$40^{\circ}\mathrm{C}$仍是饱和溶液
B.$30^{\circ}\mathrm{C}$时,在$100\mathrm{g}$水中加入$40\mathrm{g}{NaCl}$,形成不饱和溶液
C.${NaCl}$的溶解度比${Na_2CO_3}$的大
D.“夏天晒盐”经过蒸发结晶过程,“冬天捞碱”经过降温结晶过程
答案:3D
解析:
【解析】
A. 由溶解度曲线可知,${Na_{2}CO_{3}}$的溶解度随温度升高而增大,$20^{\circ}\mathrm{C}$时${Na_{2}CO_{3}}$的饱和溶液升温到$40^{\circ}\mathrm{C}$,溶解度变大,溶液变为不饱和溶液,故A错误;
B. $30^{\circ}\mathrm{C}$时${NaCl}$的溶解度小于$40\mathrm{g}$,在$100\mathrm{g}$水中加入$40\mathrm{g}{NaCl}$,不能全部溶解,形成饱和溶液,故B错误;
C. 比较物质的溶解度大小需指明温度,未指明温度无法比较${NaCl}$和${Na_{2}CO_{3}}$的溶解度大小,故C错误;
D. ${NaCl}$的溶解度受温度影响较小,“夏天晒盐”是通过蒸发结晶得到${NaCl}$;${Na_{2}CO_{3}}$的溶解度受温度影响较大,“冬天捞碱”是通过降温结晶得到${Na_{2}CO_{3}}$,故D正确。
【答案】
D
【知识点】
溶解度曲线的应用、结晶方法
【点评】
本题考查溶解度曲线的相关知识,需结合物质溶解度随温度的变化特点,分析溶液状态、结晶方法,明确比较溶解度大小必须指明温度。
【难度系数】
0.7
A. 由溶解度曲线可知,${Na_{2}CO_{3}}$的溶解度随温度升高而增大,$20^{\circ}\mathrm{C}$时${Na_{2}CO_{3}}$的饱和溶液升温到$40^{\circ}\mathrm{C}$,溶解度变大,溶液变为不饱和溶液,故A错误;
B. $30^{\circ}\mathrm{C}$时${NaCl}$的溶解度小于$40\mathrm{g}$,在$100\mathrm{g}$水中加入$40\mathrm{g}{NaCl}$,不能全部溶解,形成饱和溶液,故B错误;
C. 比较物质的溶解度大小需指明温度,未指明温度无法比较${NaCl}$和${Na_{2}CO_{3}}$的溶解度大小,故C错误;
D. ${NaCl}$的溶解度受温度影响较小,“夏天晒盐”是通过蒸发结晶得到${NaCl}$;${Na_{2}CO_{3}}$的溶解度受温度影响较大,“冬天捞碱”是通过降温结晶得到${Na_{2}CO_{3}}$,故D正确。
【答案】
D
【知识点】
溶解度曲线的应用、结晶方法
【点评】
本题考查溶解度曲线的相关知识,需结合物质溶解度随温度的变化特点,分析溶液状态、结晶方法,明确比较溶解度大小必须指明温度。
【难度系数】
0.7
4. (1)从盐卤水(含硫酸钠、氯化钠)中提取的硫酸钠可用于制中药西瓜霜,硫酸钠和氯化钠的溶解度曲线如右图所示。下列说法正确的是
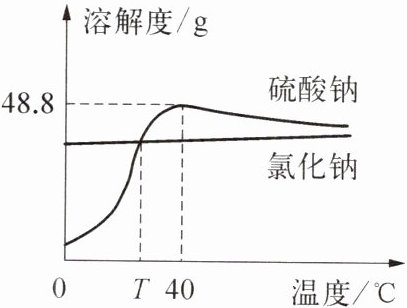
A. $40^{\circ}\mathrm{C}$时,氯化钠的溶解度是$48.8\mathrm{g}$
B. $T^{\circ}\mathrm{C}$时氯化钠溶液和硫酸钠溶液的溶质质量相等
C. 可用降温结晶的方法从盐卤水中提取硫酸钠晶体
(2)将$T^{\circ}\mathrm{C}$时的饱和硫酸钠溶液变为不饱和溶液的方法是
C
(填字母)。
A. $40^{\circ}\mathrm{C}$时,氯化钠的溶解度是$48.8\mathrm{g}$
B. $T^{\circ}\mathrm{C}$时氯化钠溶液和硫酸钠溶液的溶质质量相等
C. 可用降温结晶的方法从盐卤水中提取硫酸钠晶体
(2)将$T^{\circ}\mathrm{C}$时的饱和硫酸钠溶液变为不饱和溶液的方法是
加入溶剂(或升高温度等)
。答案:4(1)C (2)加入溶剂(或升高温度等)
解析:
【解析】
(1) 逐一分析选项:
A. 由溶解度曲线可知,40℃时,硫酸钠的溶解度是48.8g,不是氯化钠,A错误;
B. $T^{\circ}\mathrm{C}$时氯化钠和硫酸钠的溶解度相等,但未说明溶液的质量和是否饱和,无法判断溶质质量是否相等,B错误;
C. 硫酸钠的溶解度受温度影响变化较大,且温度高于40℃后溶解度随温度升高而减小,可用降温结晶的方法从盐卤水中提取硫酸钠晶体,C正确。
(2) $T^{\circ}\mathrm{C}$时,硫酸钠的溶解度随温度升高而增大,因此将该温度下的饱和硫酸钠溶液变为不饱和溶液,可采用加入溶剂或升高温度的方法。
【答案】
(1) C
(2) 加入溶剂(或升高温度等)
【知识点】
溶解度曲线应用、饱和溶液与不饱和溶液转化
【点评】
本题考查溶解度曲线的应用及饱和溶液与不饱和溶液的转化,需结合溶解度曲线的变化趋势分析,明确不同物质溶解度受温度影响的差异是解题关键。
【难度系数】
0.6
(1) 逐一分析选项:
A. 由溶解度曲线可知,40℃时,硫酸钠的溶解度是48.8g,不是氯化钠,A错误;
B. $T^{\circ}\mathrm{C}$时氯化钠和硫酸钠的溶解度相等,但未说明溶液的质量和是否饱和,无法判断溶质质量是否相等,B错误;
C. 硫酸钠的溶解度受温度影响变化较大,且温度高于40℃后溶解度随温度升高而减小,可用降温结晶的方法从盐卤水中提取硫酸钠晶体,C正确。
(2) $T^{\circ}\mathrm{C}$时,硫酸钠的溶解度随温度升高而增大,因此将该温度下的饱和硫酸钠溶液变为不饱和溶液,可采用加入溶剂或升高温度的方法。
【答案】
(1) C
(2) 加入溶剂(或升高温度等)
【知识点】
溶解度曲线应用、饱和溶液与不饱和溶液转化
【点评】
本题考查溶解度曲线的应用及饱和溶液与不饱和溶液的转化,需结合溶解度曲线的变化趋势分析,明确不同物质溶解度受温度影响的差异是解题关键。
【难度系数】
0.6