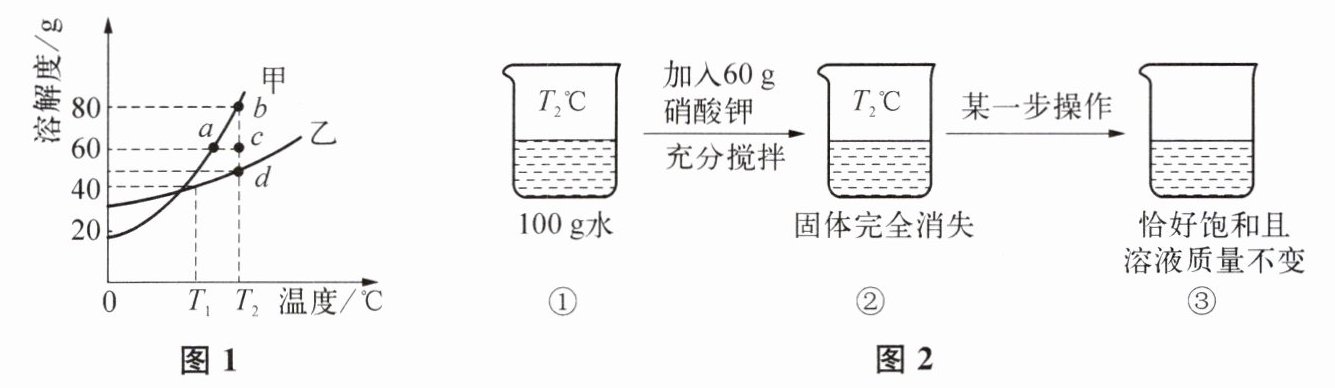
5. 甲、乙两种固体物质的溶解度曲线如图1所示:
(1)$T_1^{\circ}\mathrm{C}$时,溶解度大小关系为:甲
(2)$T_2^{\circ}\mathrm{C}$时,配制$180\mathrm{g}$甲物质的饱和溶液,需称量甲的质量
(3)由图2推测硝酸钾是图1中的
(4)图2“某一步操作”前后的溶液状态变化过程可以在图1中表示为
A. $b$点→$a$点
B. $c$点→$a$点
C. $b$点→$c$点
D. $c$点→$d$点
(5)取等质量的甲、乙两种物质,分别配制成$T_2^{\circ}\mathrm{C}$时恰好饱和的溶液,所得两种溶液的质量大小顺序为

(1)$T_1^{\circ}\mathrm{C}$时,溶解度大小关系为:甲
>
乙。(填“>”“<”或“=”)(2)$T_2^{\circ}\mathrm{C}$时,配制$180\mathrm{g}$甲物质的饱和溶液,需称量甲的质量
80
g。(3)由图2推测硝酸钾是图1中的
甲
物质。(4)图2“某一步操作”前后的溶液状态变化过程可以在图1中表示为
B
(填字母)。A. $b$点→$a$点
B. $c$点→$a$点
C. $b$点→$c$点
D. $c$点→$d$点
(5)取等质量的甲、乙两种物质,分别配制成$T_2^{\circ}\mathrm{C}$时恰好饱和的溶液,所得两种溶液的质量大小顺序为
乙>甲
。若将等质量的$T_2^{\circ}\mathrm{C}$时的甲、乙饱和溶液降温至$T_1^{\circ}\mathrm{C}$,析出固体的质量大小顺序为甲>乙
。答案:5(1)> (2)80 (3)甲 (4)B (5)乙>甲 甲>乙
解析:
【解析】
1. 由图1溶解度曲线可知,$T_1^{\circ}\mathrm{C}$时,甲的溶解度大于乙的溶解度,故填“>”。
2. $T_2^{\circ}\mathrm{C}$时甲的溶解度为80g,即100g水中溶解80g甲形成180g饱和溶液,因此配制180g甲的饱和溶液需甲的质量为80g。
3. $T_2^{\circ}\mathrm{C}$时,100g水中加入60g硝酸钾完全溶解且溶液不饱和,而该温度下甲的溶解度为80g(大于60g),乙的溶解度为60g(加入60g恰好饱和),故硝酸钾对应图1中的甲物质。
4. 图2中②是$T_2^{\circ}\mathrm{C}$时100g水溶解60g硝酸钾的不饱和溶液,对应图1的$c$点;经操作后恰好饱和且溶液质量不变,说明是降温至$T_1^{\circ}\mathrm{C}$,此时对应图1的$a$点,故变化过程为$c$点→$a$点,选B。
5. $T_2^{\circ}\mathrm{C}$时甲的溶解度大于乙,等质量的甲乙配成饱和溶液,甲所需溶剂更少,因此所得溶液质量乙>甲;等质量的$T_2^{\circ}\mathrm{C}$时的甲乙饱和溶液降温至$T_1^{\circ}\mathrm{C}$,甲的溶解度变化幅度更大,故析出固体质量甲>乙。
【答案】
(1) $\boldsymbol{>}$
(2) $\boldsymbol{80}$
(3) $\boldsymbol{甲}$
(4) $\boldsymbol{B}$
(5) $\boldsymbol{乙>甲}$;$\boldsymbol{甲>乙}$
【知识点】
溶解度曲线应用;饱和溶液判断;结晶现象
【点评】
本题结合溶解度曲线和实验操作,考查溶解度相关知识的综合应用,需准确分析曲线和实验过程的对应关系。
【难度系数】
0.6
1. 由图1溶解度曲线可知,$T_1^{\circ}\mathrm{C}$时,甲的溶解度大于乙的溶解度,故填“>”。
2. $T_2^{\circ}\mathrm{C}$时甲的溶解度为80g,即100g水中溶解80g甲形成180g饱和溶液,因此配制180g甲的饱和溶液需甲的质量为80g。
3. $T_2^{\circ}\mathrm{C}$时,100g水中加入60g硝酸钾完全溶解且溶液不饱和,而该温度下甲的溶解度为80g(大于60g),乙的溶解度为60g(加入60g恰好饱和),故硝酸钾对应图1中的甲物质。
4. 图2中②是$T_2^{\circ}\mathrm{C}$时100g水溶解60g硝酸钾的不饱和溶液,对应图1的$c$点;经操作后恰好饱和且溶液质量不变,说明是降温至$T_1^{\circ}\mathrm{C}$,此时对应图1的$a$点,故变化过程为$c$点→$a$点,选B。
5. $T_2^{\circ}\mathrm{C}$时甲的溶解度大于乙,等质量的甲乙配成饱和溶液,甲所需溶剂更少,因此所得溶液质量乙>甲;等质量的$T_2^{\circ}\mathrm{C}$时的甲乙饱和溶液降温至$T_1^{\circ}\mathrm{C}$,甲的溶解度变化幅度更大,故析出固体质量甲>乙。
【答案】
(1) $\boldsymbol{>}$
(2) $\boldsymbol{80}$
(3) $\boldsymbol{甲}$
(4) $\boldsymbol{B}$
(5) $\boldsymbol{乙>甲}$;$\boldsymbol{甲>乙}$
【知识点】
溶解度曲线应用;饱和溶液判断;结晶现象
【点评】
本题结合溶解度曲线和实验操作,考查溶解度相关知识的综合应用,需准确分析曲线和实验过程的对应关系。
【难度系数】
0.6
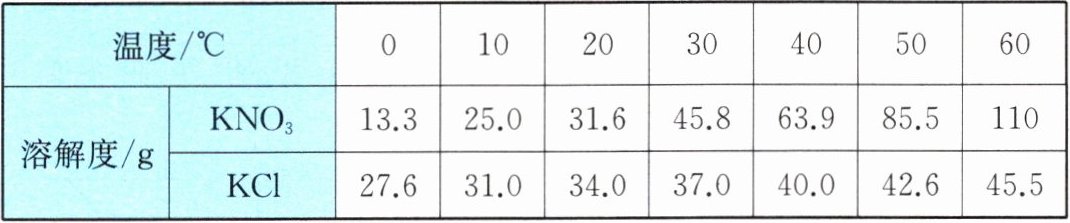
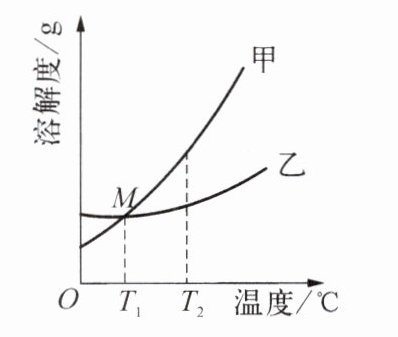
6. 已知${KNO_3}$和${KCl}$的溶解度数据如下表,溶解度曲线如下图,回答问题。
(1)图中代表${KNO_3}$溶解度曲线的是
(2)将$T_1^{\circ}\mathrm{C}$时甲和乙的饱和溶液分别升温至$T_2^{\circ}\mathrm{C}$时,溶质质量分数:甲
(3)为了将接近饱和的甲溶液变为饱和溶液,可采用的方法有
A. 加固体甲
B. 加水
C. 降低温度
D. 蒸发溶剂
(4)参照表中数据,交点$M$的取值范围正确的是
A. $10∼20^{\circ}\mathrm{C}$
B. $20∼30^{\circ}\mathrm{C}$
C. $30∼40^{\circ}\mathrm{C}$
D. $40∼50^{\circ}\mathrm{C}$


(1)图中代表${KNO_3}$溶解度曲线的是
甲
(填“甲”或“乙”)。(2)将$T_1^{\circ}\mathrm{C}$时甲和乙的饱和溶液分别升温至$T_2^{\circ}\mathrm{C}$时,溶质质量分数:甲
=
乙。(填“>”“=”或“<”)(3)为了将接近饱和的甲溶液变为饱和溶液,可采用的方法有
ACD
(填字母,下同)。A. 加固体甲
B. 加水
C. 降低温度
D. 蒸发溶剂
(4)参照表中数据,交点$M$的取值范围正确的是
B
。A. $10∼20^{\circ}\mathrm{C}$
B. $20∼30^{\circ}\mathrm{C}$
C. $30∼40^{\circ}\mathrm{C}$
D. $40∼50^{\circ}\mathrm{C}$
答案:6(1)甲 (2)= (3)ACD (4)B
解析:
【解析】
(1) 由溶解度数据可知,KNO₃的溶解度受温度影响变化较大,所以图中代表KNO₃溶解度曲线的是甲。
(2) T₁℃时,甲和乙的溶解度相等,其饱和溶液的溶质质量分数相等;升温至T₂℃时,甲、乙的溶解度均增大,饱和溶液变为不饱和溶液,溶质质量分数均不变,故溶质质量分数:甲=乙。
(3) 甲的溶解度随温度升高而增大,将接近饱和的甲溶液变为饱和溶液,可采用加固体甲、降低温度、蒸发溶剂的方法,加水会使溶液更不饱和,故选ACD。
(4) 由表格数据可知,20℃时,KNO₃溶解度为31.6g,KCl溶解度为34.0g;30℃时,KNO₃溶解度为45.8g,KCl溶解度为37.0g,说明在20~30℃之间,二者溶解度相等,即交点M的取值范围是20~30℃,故选B。
【答案】
(1) 甲
(2) =
(3) ACD
(4) B
【知识点】
溶解度曲线的应用;饱和溶液与不饱和溶液的转化;溶质质量分数比较
【点评】
本题围绕溶解度曲线与溶解度数据展开,考查了溶解度曲线的判断、溶质质量分数变化、饱和溶液与不饱和溶液的转化等知识点,需结合溶解度随温度的变化规律分析解决问题。
【难度系数】
0.6
(1) 由溶解度数据可知,KNO₃的溶解度受温度影响变化较大,所以图中代表KNO₃溶解度曲线的是甲。
(2) T₁℃时,甲和乙的溶解度相等,其饱和溶液的溶质质量分数相等;升温至T₂℃时,甲、乙的溶解度均增大,饱和溶液变为不饱和溶液,溶质质量分数均不变,故溶质质量分数:甲=乙。
(3) 甲的溶解度随温度升高而增大,将接近饱和的甲溶液变为饱和溶液,可采用加固体甲、降低温度、蒸发溶剂的方法,加水会使溶液更不饱和,故选ACD。
(4) 由表格数据可知,20℃时,KNO₃溶解度为31.6g,KCl溶解度为34.0g;30℃时,KNO₃溶解度为45.8g,KCl溶解度为37.0g,说明在20~30℃之间,二者溶解度相等,即交点M的取值范围是20~30℃,故选B。
【答案】
(1) 甲
(2) =
(3) ACD
(4) B
【知识点】
溶解度曲线的应用;饱和溶液与不饱和溶液的转化;溶质质量分数比较
【点评】
本题围绕溶解度曲线与溶解度数据展开,考查了溶解度曲线的判断、溶质质量分数变化、饱和溶液与不饱和溶液的转化等知识点,需结合溶解度随温度的变化规律分析解决问题。
【难度系数】
0.6