1. 下列四种物质中,属于溶液的是(
A.牛奶
B.黄泥水
C.冰水共存物
D.澄清石灰水
D
)A.牛奶
B.黄泥水
C.冰水共存物
D.澄清石灰水
答案:1. D
解析:
【解析】
溶液是均一、稳定的混合物。
A.牛奶是乳浊液,不均一、不稳定,不属于溶液;
B.黄泥水是悬浊液,不均一、不稳定,不属于溶液;
C.冰水共存物只由水一种物质组成,属于纯净物,不属于溶液;
D.澄清石灰水是氢氧化钙溶于水形成的均一、稳定的混合物,属于溶液。
【答案】
D
【知识点】
溶液的定义、浊液与溶液区分、纯净物与混合物判断
【点评】
本题考查溶液的基本特征,需区分溶液、浊液及纯净物,属于基础题型,要求学生熟练掌握溶液均一、稳定的特点及混合物的概念。
【难度系数】
0.8
溶液是均一、稳定的混合物。
A.牛奶是乳浊液,不均一、不稳定,不属于溶液;
B.黄泥水是悬浊液,不均一、不稳定,不属于溶液;
C.冰水共存物只由水一种物质组成,属于纯净物,不属于溶液;
D.澄清石灰水是氢氧化钙溶于水形成的均一、稳定的混合物,属于溶液。
【答案】
D
【知识点】
溶液的定义、浊液与溶液区分、纯净物与混合物判断
【点评】
本题考查溶液的基本特征,需区分溶液、浊液及纯净物,属于基础题型,要求学生熟练掌握溶液均一、稳定的特点及混合物的概念。
【难度系数】
0.8
2. 溶液与人们的生活息息相关,下列溶液中溶剂不是水的是(
A.碘酒
B.生理盐水
C.医用酒精
D.白醋
A
)A.碘酒
B.生理盐水
C.医用酒精
D.白醋
答案:2. A
解析:
【解析】
逐一分析各选项:
A. 碘酒是碘的酒精溶液,溶剂是酒精(乙醇),不是水;
B. 生理盐水是氯化钠的水溶液,溶剂是水;
C. 医用酒精是酒精的水溶液,溶剂是水;
D. 白醋是醋酸的水溶液,溶剂是水。
因此溶剂不是水的是碘酒,选A。
【答案】
A
【知识点】
溶液的组成、溶剂判断
【点评】
本题考查常见溶液中溶剂的判断,需要熟悉生活中常见溶液的成分,属于基础题。
【难度系数】
0.8
逐一分析各选项:
A. 碘酒是碘的酒精溶液,溶剂是酒精(乙醇),不是水;
B. 生理盐水是氯化钠的水溶液,溶剂是水;
C. 医用酒精是酒精的水溶液,溶剂是水;
D. 白醋是醋酸的水溶液,溶剂是水。
因此溶剂不是水的是碘酒,选A。
【答案】
A
【知识点】
溶液的组成、溶剂判断
【点评】
本题考查常见溶液中溶剂的判断,需要熟悉生活中常见溶液的成分,属于基础题。
【难度系数】
0.8
3. 下列是关于溶液、悬浊液、乳浊液的说法,其中正确的是(
① 溶液一定是无色、透明的液体;② 溶液是纯净物,而浊液是混合物;③ 物质在溶液中以分子或离子的形式存在;④ 泥浆水是悬浊液
A.①②
B.①③
C.②③
D.③④
D
)① 溶液一定是无色、透明的液体;② 溶液是纯净物,而浊液是混合物;③ 物质在溶液中以分子或离子的形式存在;④ 泥浆水是悬浊液
A.①②
B.①③
C.②③
D.③④
答案:3. D
解析:
【解析】
逐一分析各说法:
① 溶液不一定是无色的,如硫酸铜溶液为蓝色,该说法错误;
② 溶液、悬浊液、乳浊液均属于混合物,该说法错误;
③ 物质在溶液中以分子或离子的形式均匀分散,该说法正确;
④ 泥浆水是固体小颗粒分散在水中形成的悬浊液,该说法正确。
综上,正确的是③④,故选D。
【答案】
D
【知识点】
溶液的特征、浊液的分类、溶液与浊液的区别
【点评】
本题考查溶液、悬浊液、乳浊液的基本概念与特征,需明确溶液不一定无色、溶液与浊液均为混合物等易混淆点,侧重对基础概念的理解与应用。
【难度系数】
0.7
逐一分析各说法:
① 溶液不一定是无色的,如硫酸铜溶液为蓝色,该说法错误;
② 溶液、悬浊液、乳浊液均属于混合物,该说法错误;
③ 物质在溶液中以分子或离子的形式均匀分散,该说法正确;
④ 泥浆水是固体小颗粒分散在水中形成的悬浊液,该说法正确。
综上,正确的是③④,故选D。
【答案】
D
【知识点】
溶液的特征、浊液的分类、溶液与浊液的区别
【点评】
本题考查溶液、悬浊液、乳浊液的基本概念与特征,需明确溶液不一定无色、溶液与浊液均为混合物等易混淆点,侧重对基础概念的理解与应用。
【难度系数】
0.7
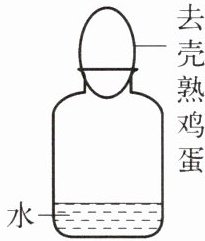
4. 如右图所示,要想将去壳的熟鸡蛋吸入瓶中,可以向装有水的瓶中加入的物质是(
A.硝酸铵
B.生石灰
C.浓硫酸
D.烧碱
A
)
A.硝酸铵
B.生石灰
C.浓硫酸
D.烧碱
答案:4. A
解析:
【解析】
要将去壳熟鸡蛋吸入瓶中,需使瓶内压强小于外界大气压。
A. 硝酸铵溶于水时吸收热量,瓶内温度降低,瓶内气体遇冷收缩,压强减小,小于外界大气压,能将鸡蛋吸入瓶中,符合要求;
B. 生石灰与水反应放出大量热,瓶内温度升高,气体膨胀,压强增大,鸡蛋会被推出,不符合要求;
C. 浓硫酸溶于水放出大量热,瓶内压强增大,鸡蛋会被推出,不符合要求;
D. 烧碱(氢氧化钠)溶于水放出大量热,瓶内压强增大,鸡蛋会被推出,不符合要求。
【答案】
A
【知识点】
溶解时的吸放热现象;气体压强与温度的关系
【点评】
本题考查物质溶于水或与水反应时的热量变化对瓶内压强的影响,需明确吸热过程使瓶内压强减小、放热过程使瓶内压强增大,结合实验现象分析判断。
【难度系数】
0.6
要将去壳熟鸡蛋吸入瓶中,需使瓶内压强小于外界大气压。
A. 硝酸铵溶于水时吸收热量,瓶内温度降低,瓶内气体遇冷收缩,压强减小,小于外界大气压,能将鸡蛋吸入瓶中,符合要求;
B. 生石灰与水反应放出大量热,瓶内温度升高,气体膨胀,压强增大,鸡蛋会被推出,不符合要求;
C. 浓硫酸溶于水放出大量热,瓶内压强增大,鸡蛋会被推出,不符合要求;
D. 烧碱(氢氧化钠)溶于水放出大量热,瓶内压强增大,鸡蛋会被推出,不符合要求。
【答案】
A
【知识点】
溶解时的吸放热现象;气体压强与温度的关系
【点评】
本题考查物质溶于水或与水反应时的热量变化对瓶内压强的影响,需明确吸热过程使瓶内压强减小、放热过程使瓶内压强增大,结合实验现象分析判断。
【难度系数】
0.6
5. 用400g溶质质量分数为20%的氢氧化钠溶液,配制成溶质质量分数为10%的氢氧化钠溶液,需要加入水的质量是(
A.100g
B.200g
C.400g
D.800g
C
)A.100g
B.200g
C.400g
D.800g
答案:5. C
解析:
【解析】
设需要加入水的质量是$x$。
根据溶液稀释前后溶质的质量不变,可得:
$400g×20\%=(400g + x)×10\%$
$80g=(400g + x)×10\%$
$400g + x=\frac{80g}{10\%}$
$400g + x = 800g$
$x = 800g - 400g$
$x = 400g$
【答案】
C
【知识点】
溶液的稀释、溶质质量分数的计算
【点评】
本题考查溶液稀释的计算,关键是掌握溶液稀释前后溶质质量不变这一原理。
【难度系数】
0.6
设需要加入水的质量是$x$。
根据溶液稀释前后溶质的质量不变,可得:
$400g×20\%=(400g + x)×10\%$
$80g=(400g + x)×10\%$
$400g + x=\frac{80g}{10\%}$
$400g + x = 800g$
$x = 800g - 400g$
$x = 400g$
【答案】
C
【知识点】
溶液的稀释、溶质质量分数的计算
【点评】
本题考查溶液稀释的计算,关键是掌握溶液稀释前后溶质质量不变这一原理。
【难度系数】
0.6
6. 实验室配制一定溶质质量分数的氯化钠溶液时,下列操作会导致结果偏大的是(
A.氯化钠固体中含有杂质
B.用量筒量取水时仰视读数
C.加水溶解固体时有水洒出
D.配制好的溶液装瓶时有少量洒出
C
)A.氯化钠固体中含有杂质
B.用量筒量取水时仰视读数
C.加水溶解固体时有水洒出
D.配制好的溶液装瓶时有少量洒出
答案:6. C
解析:
【解析】
溶质质量分数 = 溶质质量/溶液质量×100%,据此分析各选项:
A. 氯化钠固体中含有杂质,会使实际溶质质量偏小,溶剂质量不变,溶质质量分数偏小,不符合题意;
B. 用量筒量取水时仰视读数,会导致量取的水的实际体积偏大,溶质质量不变,溶液质量偏大,溶质质量分数偏小,不符合题意;
C. 加水溶解固体时有水洒出,会使实际溶剂质量偏小,溶质质量不变,溶液质量偏小,溶质质量分数偏大,符合题意;
D. 溶液具有均一性,配制好的溶液装瓶时有少量洒出,溶质质量分数不变,不符合题意。
【答案】
C
【知识点】
配制溶液误差分析;溶质质量分数计算
【点评】
本题考查配制一定溶质质量分数溶液的误差分析,需结合溶质质量分数公式,分析操作对溶质、溶剂质量的影响,明确溶液的均一性是解题关键,侧重对基础知识的考查。
【难度系数】
0.6
溶质质量分数 = 溶质质量/溶液质量×100%,据此分析各选项:
A. 氯化钠固体中含有杂质,会使实际溶质质量偏小,溶剂质量不变,溶质质量分数偏小,不符合题意;
B. 用量筒量取水时仰视读数,会导致量取的水的实际体积偏大,溶质质量不变,溶液质量偏大,溶质质量分数偏小,不符合题意;
C. 加水溶解固体时有水洒出,会使实际溶剂质量偏小,溶质质量不变,溶液质量偏小,溶质质量分数偏大,符合题意;
D. 溶液具有均一性,配制好的溶液装瓶时有少量洒出,溶质质量分数不变,不符合题意。
【答案】
C
【知识点】
配制溶液误差分析;溶质质量分数计算
【点评】
本题考查配制一定溶质质量分数溶液的误差分析,需结合溶质质量分数公式,分析操作对溶质、溶剂质量的影响,明确溶液的均一性是解题关键,侧重对基础知识的考查。
【难度系数】
0.6
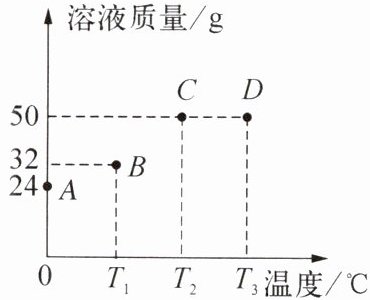
7. 将34g晶体W(不含结晶水)投入盛有16g不同温度水的烧杯中(忽略溶解吸、放热),充分溶解,测得0℃、T₁℃、T₂℃、T₃℃的烧杯中溶液的质量分别如图中点A、B、C、D所示。下列说法错误的是(
A.在0~T₂℃范围内,晶体W的溶解度随温度升高而增大
B.T₁℃时,晶体W的溶解度是100g
C.B、C两点对应的溶液中,溶质质量分数较大的是C
D.A、B、C、D四点所对应的溶液中,属于饱和溶液的是B、C
D
)
A.在0~T₂℃范围内,晶体W的溶解度随温度升高而增大
B.T₁℃时,晶体W的溶解度是100g
C.B、C两点对应的溶液中,溶质质量分数较大的是C
D.A、B、C、D四点所对应的溶液中,属于饱和溶液的是B、C
答案:7. D
解析:
解:
A. 0℃时溶液质量24g,溶解溶质24g-16g=8g;T₂℃时溶液质量50g,溶解溶质50g-16g=34g,温度升高溶解溶质增多,溶解度随温度升高而增大,A正确。
B. T₁℃时溶液质量32g,溶解溶质32g-16g=16g,溶剂16g,溶解度$S=\frac{16g}{16g}×100g=100g$,B正确。
C. B点溶质16g、溶液32g,质量分数$\frac{16}{32}×100\% = 50\%$;C点溶质34g、溶液50g,质量分数$\frac{34}{50}×100\%=68\%$,C点较大,C正确。
D. A点溶解8g未达34g,不饱和;B点溶解16g未达34g(T₁℃溶解度100g,16g水最多溶16g),饱和;C点溶解34g达最大,饱和;D点温度高于T₂℃,溶液质量50g与C点相同,溶质34g,可能不饱和,D错误。
答案:D
A. 0℃时溶液质量24g,溶解溶质24g-16g=8g;T₂℃时溶液质量50g,溶解溶质50g-16g=34g,温度升高溶解溶质增多,溶解度随温度升高而增大,A正确。
B. T₁℃时溶液质量32g,溶解溶质32g-16g=16g,溶剂16g,溶解度$S=\frac{16g}{16g}×100g=100g$,B正确。
C. B点溶质16g、溶液32g,质量分数$\frac{16}{32}×100\% = 50\%$;C点溶质34g、溶液50g,质量分数$\frac{34}{50}×100\%=68\%$,C点较大,C正确。
D. A点溶解8g未达34g,不饱和;B点溶解16g未达34g(T₁℃溶解度100g,16g水最多溶16g),饱和;C点溶解34g达最大,饱和;D点温度高于T₂℃,溶液质量50g与C点相同,溶质34g,可能不饱和,D错误。
答案:D