8. 20℃时,将一定质量的甲、乙两种溶液进行恒温蒸发,蒸发溶剂的质量与析出晶体的质量关系如图所示(图中两线相交于c点)。下列分析错误的是(
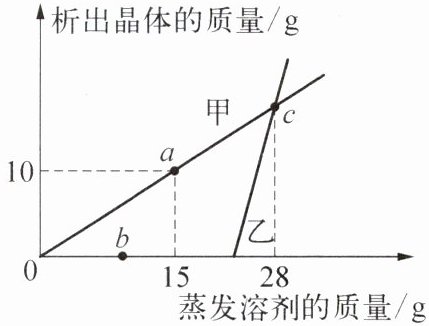
A.20℃时,b点对应的乙溶液是不饱和溶液
B.20℃时,对甲、乙两种溶液恒温蒸发28g溶剂,两者析出晶体的质量相等
C.20℃时,等质量的甲、乙两种饱和溶液中,溶质质量:乙>甲
D.20℃时,甲的饱和溶液溶质质量分数为25%
D
)
A.20℃时,b点对应的乙溶液是不饱和溶液
B.20℃时,对甲、乙两种溶液恒温蒸发28g溶剂,两者析出晶体的质量相等
C.20℃时,等质量的甲、乙两种饱和溶液中,溶质质量:乙>甲
D.20℃时,甲的饱和溶液溶质质量分数为25%
答案:8. D
解析:
A. 由图可知,乙溶液蒸发一定质量溶剂后才开始析出晶体,b点未达此质量,故为不饱和溶液,正确。
B. c点对应蒸发28g溶剂,两线相交,析出晶体质量相等,正确。
C. 饱和时,乙析出晶体速率更快,溶解度更大,等质量饱和溶液中溶质质量乙>甲,正确。
D. 甲溶液蒸发15g溶剂析出10g晶体达饱和,设溶解度为$S$,$\frac{S}{100g}=\frac{10g}{15g}$,$S=\frac{200}{3}g$,溶质质量分数$=\frac{\frac{200}{3}g}{100g+\frac{200}{3}g}×100\%\approx40\%\neq25\%$,错误。
答案:D
B. c点对应蒸发28g溶剂,两线相交,析出晶体质量相等,正确。
C. 饱和时,乙析出晶体速率更快,溶解度更大,等质量饱和溶液中溶质质量乙>甲,正确。
D. 甲溶液蒸发15g溶剂析出10g晶体达饱和,设溶解度为$S$,$\frac{S}{100g}=\frac{10g}{15g}$,$S=\frac{200}{3}g$,溶质质量分数$=\frac{\frac{200}{3}g}{100g+\frac{200}{3}g}×100\%\approx40\%\neq25\%$,错误。
答案:D
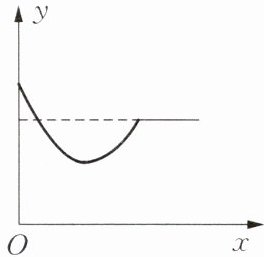
9. 一定温度下,向饱和石灰水中加入下列哪种固体后,溶液中的溶质质量随时间的变化关系如右图所示(
A.生石灰
B.硝酸铵
C.氢氧化钙
D.氢氧化钠
A
)
A.生石灰
B.硝酸铵
C.氢氧化钙
D.氢氧化钠
答案:9. A
解析:
【解析】
分析图像可知,溶液中溶质质量先减小,后增大至原饱和溶液的溶质质量,最终保持不变。对各选项分析如下:
A. 生石灰(CaO):加入饱和石灰水后,CaO与水反应生成Ca(OH)₂,反应消耗溶剂水,且反应放热使溶液温度升高,氢氧化钙的溶解度随温度升高而减小,因此有溶质析出,溶质质量减小;待反应结束,温度恢复至室温,溶解度恢复,析出的氢氧化钙部分溶解,最终溶质质量回到原水平,符合图像。
B. 硝酸铵:溶于水吸热,溶液温度降低,氢氧化钙溶解度随温度降低而增大,饱和溶液中会溶解更多溶质,溶质质量增大,与图像不符。
C. 氢氧化钙:饱和石灰水不能继续溶解氢氧化钙,溶质质量始终不变,与图像不符。
D. 氢氧化钠:溶于水放热,溶液温度升高,氢氧化钙溶解度减小,溶质析出,质量减小;但氢氧化钠不消耗溶剂,温度恢复后,溶质质量虽能恢复,但整个过程无溶剂减少导致的变化特征,与图像不符。
【答案】
A
【知识点】
饱和溶液性质,氢氧化钙溶解度特性,生石灰与水反应
【点评】
本题结合图像考查饱和石灰水的相关性质,需综合分析物质与水的反应、溶解吸放热对溶解度的影响,明确溶液中溶质质量的变化过程是解题关键。
【难度系数】
0.6
分析图像可知,溶液中溶质质量先减小,后增大至原饱和溶液的溶质质量,最终保持不变。对各选项分析如下:
A. 生石灰(CaO):加入饱和石灰水后,CaO与水反应生成Ca(OH)₂,反应消耗溶剂水,且反应放热使溶液温度升高,氢氧化钙的溶解度随温度升高而减小,因此有溶质析出,溶质质量减小;待反应结束,温度恢复至室温,溶解度恢复,析出的氢氧化钙部分溶解,最终溶质质量回到原水平,符合图像。
B. 硝酸铵:溶于水吸热,溶液温度降低,氢氧化钙溶解度随温度降低而增大,饱和溶液中会溶解更多溶质,溶质质量增大,与图像不符。
C. 氢氧化钙:饱和石灰水不能继续溶解氢氧化钙,溶质质量始终不变,与图像不符。
D. 氢氧化钠:溶于水放热,溶液温度升高,氢氧化钙溶解度减小,溶质析出,质量减小;但氢氧化钠不消耗溶剂,温度恢复后,溶质质量虽能恢复,但整个过程无溶剂减少导致的变化特征,与图像不符。
【答案】
A
【知识点】
饱和溶液性质,氢氧化钙溶解度特性,生石灰与水反应
【点评】
本题结合图像考查饱和石灰水的相关性质,需综合分析物质与水的反应、溶解吸放热对溶解度的影响,明确溶液中溶质质量的变化过程是解题关键。
【难度系数】
0.6
10. 运城盐湖是三大内陆盐湖之一。当地人们通过“冬天捞碱,夏天晒盐”的方式获得大量湖盐,为探究其原理,创新小组的同学设计了以下实验。结合表格信息,下列分析正确的是(

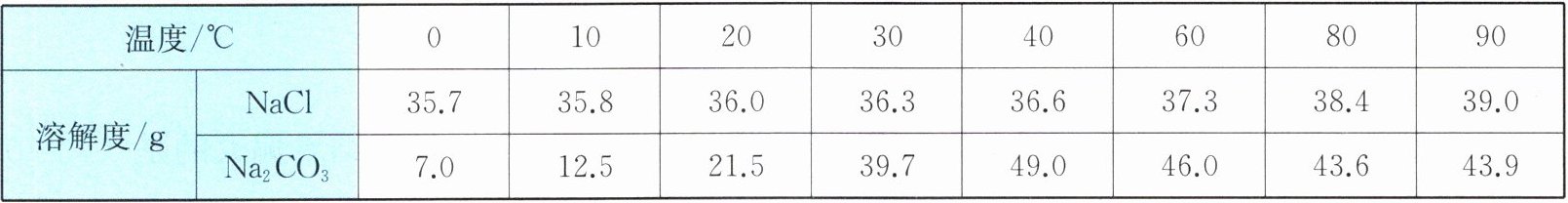
A.①中玻璃棒的作用是散热
B.②中析出晶体的操作为降温结晶
C.③的溶液为碳酸钠的饱和溶液
D.④中析出的晶体全部为碳酸钠
C
)

A.①中玻璃棒的作用是散热
B.②中析出晶体的操作为降温结晶
C.③的溶液为碳酸钠的饱和溶液
D.④中析出的晶体全部为碳酸钠
答案:10. C
解析:
【解析】
A. ①为溶解操作,玻璃棒的作用是搅拌以加速溶解,并非散热,A错误;
B. 氯化钠溶解度受温度影响较小,②中析出氯化钠晶体的操作为蒸发结晶,而非降温结晶,B错误;
C. ③中有碳酸钠晶体析出,说明该溶液无法继续溶解碳酸钠,属于碳酸钠的饱和溶液,C正确;
D. ④中降温后,碳酸钠溶解度骤降析出晶体,但氯化钠在该温度下也可能达到饱和状态析出部分晶体,因此析出的晶体并非全部为碳酸钠,D错误。
【答案】
C
【知识点】
溶解度的应用;结晶方法;饱和溶液判断
【点评】
本题结合生活中“冬天捞碱,夏天晒盐”的实际场景,考查溶解度、结晶方法及饱和溶液的相关知识,要求学生能结合物质溶解度受温度影响的差异分析实际问题,侧重知识的应用能力考查。
【难度系数】
0.6
A. ①为溶解操作,玻璃棒的作用是搅拌以加速溶解,并非散热,A错误;
B. 氯化钠溶解度受温度影响较小,②中析出氯化钠晶体的操作为蒸发结晶,而非降温结晶,B错误;
C. ③中有碳酸钠晶体析出,说明该溶液无法继续溶解碳酸钠,属于碳酸钠的饱和溶液,C正确;
D. ④中降温后,碳酸钠溶解度骤降析出晶体,但氯化钠在该温度下也可能达到饱和状态析出部分晶体,因此析出的晶体并非全部为碳酸钠,D错误。
【答案】
C
【知识点】
溶解度的应用;结晶方法;饱和溶液判断
【点评】
本题结合生活中“冬天捞碱,夏天晒盐”的实际场景,考查溶解度、结晶方法及饱和溶液的相关知识,要求学生能结合物质溶解度受温度影响的差异分析实际问题,侧重知识的应用能力考查。
【难度系数】
0.6
11. 溶质质量分数为10%的氯化钠溶液对葡萄球菌具有明显的抑制效果。图1、图2为配制氯化钠杀菌液的过程,结合下表NaCl的溶解度数据,下列有关分析正确的是(
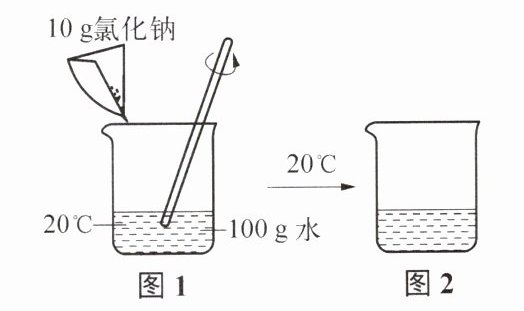

A.图1中搅拌可增大氯化钠的溶解度
B.图2中溶液为20℃时氯化钠的不饱和溶液
C.图2中溶液对葡萄球菌有明显的杀菌效果
D.从氯化钠溶液中得到氯化钠晶体常采用降温结晶的方法
B
)

A.图1中搅拌可增大氯化钠的溶解度
B.图2中溶液为20℃时氯化钠的不饱和溶液
C.图2中溶液对葡萄球菌有明显的杀菌效果
D.从氯化钠溶液中得到氯化钠晶体常采用降温结晶的方法
答案:11. B
解析:
【解析】
A. 搅拌只能加快氯化钠的溶解速率,溶解度仅与温度、溶质和溶剂的性质有关,搅拌不能增大溶解度,故A错误;
B. 20℃时NaCl的溶解度为36g,即100g水中最多溶解36gNaCl,则80g水中最多溶解$\frac{36g}{100g}×80g=28.8g$NaCl,图2中加入的NaCl质量为8g,远小于28.8g,因此该溶液为20℃时氯化钠的不饱和溶液,故B正确;
C. 图2中溶液的溶质质量分数为$\frac{8g}{80g+8g}×100\%≈9.09\%$,小于10%,对葡萄球菌没有明显的杀菌效果,故C错误;
D. 氯化钠的溶解度受温度影响较小,从氯化钠溶液中得到氯化钠晶体常采用蒸发结晶的方法,而非降温结晶,故D错误。
【答案】
B
【知识点】
固体溶解度的影响因素、饱和溶液与不饱和溶液判断、溶质质量分数计算
【点评】
本题结合溶液配制过程,综合考查固体溶解度、饱和溶液判断、溶质质量分数计算及结晶方法等知识点,需结合数据分析判断,注重对基础知识的综合应用能力。
【难度系数】
0.6
A. 搅拌只能加快氯化钠的溶解速率,溶解度仅与温度、溶质和溶剂的性质有关,搅拌不能增大溶解度,故A错误;
B. 20℃时NaCl的溶解度为36g,即100g水中最多溶解36gNaCl,则80g水中最多溶解$\frac{36g}{100g}×80g=28.8g$NaCl,图2中加入的NaCl质量为8g,远小于28.8g,因此该溶液为20℃时氯化钠的不饱和溶液,故B正确;
C. 图2中溶液的溶质质量分数为$\frac{8g}{80g+8g}×100\%≈9.09\%$,小于10%,对葡萄球菌没有明显的杀菌效果,故C错误;
D. 氯化钠的溶解度受温度影响较小,从氯化钠溶液中得到氯化钠晶体常采用蒸发结晶的方法,而非降温结晶,故D错误。
【答案】
B
【知识点】
固体溶解度的影响因素、饱和溶液与不饱和溶液判断、溶质质量分数计算
【点评】
本题结合溶液配制过程,综合考查固体溶解度、饱和溶液判断、溶质质量分数计算及结晶方法等知识点,需结合数据分析判断,注重对基础知识的综合应用能力。
【难度系数】
0.6