1.
镁、铝、锌、铁
等活动性较强的金属能与稀盐酸、稀硫酸发生置换反应,放出氢气
,同时生成一类称为盐
的化合物。如镁与稀硫酸反应的化学方程式为$\mathrm{M g + H_2SO_4 \xlongequal{ } MgSO_4 + H_2 \uparrow}$
,铝与稀盐酸反应的化学方程式为$\mathrm{2A l + 6HCl \xlongequal{ } 2AlCl_3 + 3H_2 \uparrow}$
。还有一些活动性较弱的金属(如铜
)不能与稀盐酸或稀硫酸发生置换反应。答案:1.镁、铝、锌、铁 氢气 盐 $\mathrm{M g + H_2SO_4 \xlongequal{ } MgSO_4 + H_2 \uparrow}$ $\mathrm{2A l + 6HCl \xlongequal{ } 2AlCl_3 + 3H_2 \uparrow}$ 铜
2. 金属单质能否与酸发生置换反应、反应的难易程度如何,与金属的
活动性强弱
有关。经进一步研究可知,常见金属的活动性顺序为K、Ca、Na、Mg、Al、Zn、Fe、Sn、Pb
(H)Cu、Hg、Ag、Pt、Au
。答案:2.活动性强弱 K、Ca、Na、Mg、Al、Zn、Fe、Sn、Pb Cu、Hg、Ag、Pt、Au
3. 稀盐酸、稀硫酸还能与金属氧化物反应,生成
盐
和水
。如氧化铜与稀硫酸反应的化学方程式为$\mathrm{CuO + H_2SO_4 \xlongequal{ } CuSO_4 + H_2O}$
,氧化铁与稀盐酸反应的化学方程式为$\mathrm{Fe_2O_3 + 6HCl \xlongequal{ } 2FeCl_3 + 3H_2O}$
。答案:3.盐 水 $\mathrm{CuO + H_2SO_4 \xlongequal{ } CuSO_4 + H_2O}$ $\mathrm{Fe_2O_3 + 6HCl \xlongequal{ } 2FeCl_3 + 3H_2O}$
1. 下列金属中不能与稀硫酸发生置换反应放出氢气的是(
A.镁
B.铝
C.铁
D.铜
D
)A.镁
B.铝
C.铁
D.铜
答案:1.D
2. 下列有关硫酸的认识或做法,正确的是(
A.性质:能与CO₂发生反应
B.组成:硫酸中H⁺和SO₄²⁻的数目相同
C.用途:用于生产化肥、农药、染料等
D.生产:含硫酸的工业废水,可以直接排放
C
)A.性质:能与CO₂发生反应
B.组成:硫酸中H⁺和SO₄²⁻的数目相同
C.用途:用于生产化肥、农药、染料等
D.生产:含硫酸的工业废水,可以直接排放
答案:2.C
3. 现有四种物质:①FeCl₃;②FeCl₂;③CuCl₂;④AlCl₃,其中能用金属与稀盐酸直接反应制得的物质是(
A.①②
B.②④
C.③④
D.①③
B
)A.①②
B.②④
C.③④
D.①③
答案:3.B
4. 把过量稀盐酸加入装有下列固体的烧杯中,能得到无色澄清溶液的是(
A.氧化铜
B.氧化铁
C.镁
D.铁
C
)A.氧化铜
B.氧化铁
C.镁
D.铁
答案:4.C
5. 右图中化学反应的溶液颜色变化体现了“魔法世界,魅力化学”。请回答:
(1)溶液X为
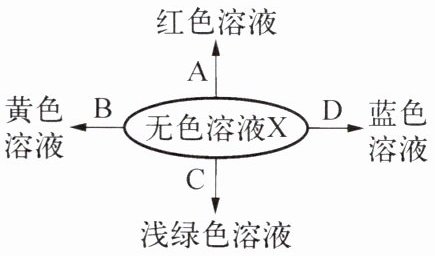
(2)若X是稀硫酸,B是氧化物,则B的化学式为
(3)若X是稀盐酸,C是单质,则C的化学式为
(4)若X是稀盐酸,D是氧化物,则D应该是一种
(1)溶液X为
酸性
(填“酸性”或“碱性”)溶液,试剂A的名称是紫色石蕊溶液
。
(2)若X是稀硫酸,B是氧化物,则B的化学式为
$\mathrm{Fe_2O_3}$
。(3)若X是稀盐酸,C是单质,则C的化学式为
Fe
,该反应属于置换
(填基本反应类型)反应。(4)若X是稀盐酸,D是氧化物,则D应该是一种
黑
色固体,X与D反应的化学方程式为$\mathrm{CuO + 2HCl \xlongequal{ } CuCl_2 + H_2O}$
。答案:5.(1) 酸性 紫色石蕊溶液 (2) $\mathrm{Fe_2O_3}$ (3) Fe 置换 (4) 黑 $\mathrm{CuO + 2HCl \xlongequal{ } CuCl_2 + H_2O}$