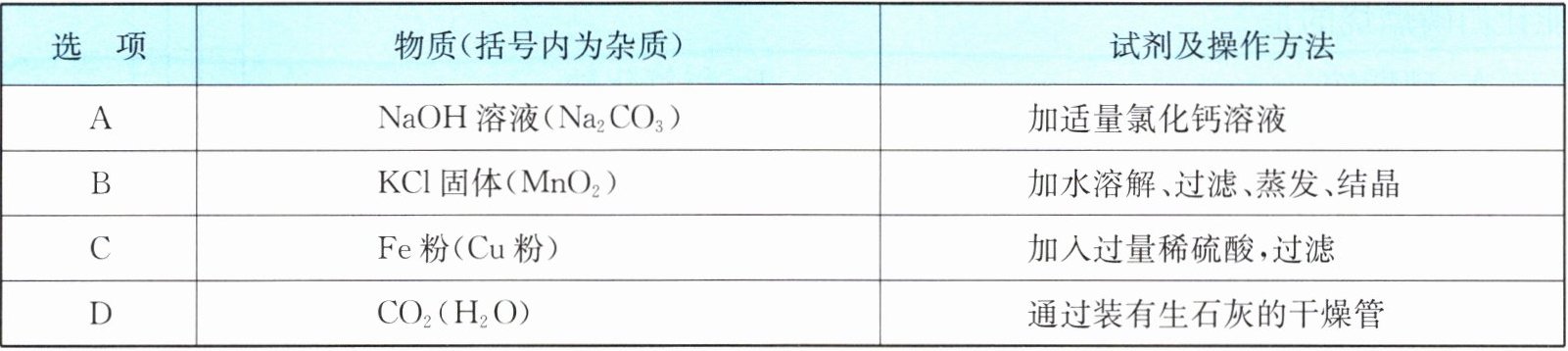
14. 除去下列物质中混有的少量杂质,所选用的试剂及操作方法正确的是(
B
)
答案:14. B
解析:
解:A. 加入适量氯化钙溶液,碳酸钠与氯化钙反应生成碳酸钙沉淀和氯化钠,引入新杂质氯化钠,错误。
B. KCl易溶于水,MnO₂难溶于水,加水溶解、过滤除去MnO₂,蒸发结晶得到KCl固体,正确。
C. 加入过量稀硫酸,铁粉与稀硫酸反应,铜粉不反应,除去了原物质,错误。
D. 生石灰与水反应生成氢氧化钙,氢氧化钙与二氧化碳反应,除去了原物质,错误。
结论:正确选项为B。
B. KCl易溶于水,MnO₂难溶于水,加水溶解、过滤除去MnO₂,蒸发结晶得到KCl固体,正确。
C. 加入过量稀硫酸,铁粉与稀硫酸反应,铜粉不反应,除去了原物质,错误。
D. 生石灰与水反应生成氢氧化钙,氢氧化钙与二氧化碳反应,除去了原物质,错误。
结论:正确选项为B。
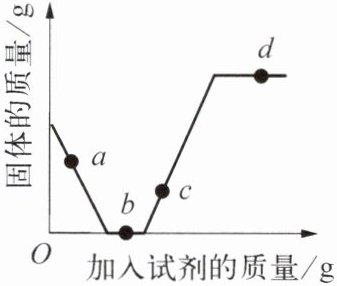
15. 向一定质量的 $Fe_2O_3$ 中滴加稀盐酸,一段时间后,改为滴加 $NaOH$ 溶液,固体质量随加入试剂质量的变化趋势如右图所示。下列有关说法错误的是(
A.$a$ 点时溶液中一定存在 $Fe^{3+}$
B.$b$ 点时所加试剂一定是稀盐酸
C.$c$ 点时固体的颜色是红褐色
D.$d$ 点时溶液中有两种溶质
B
)
A.$a$ 点时溶液中一定存在 $Fe^{3+}$
B.$b$ 点时所加试剂一定是稀盐酸
C.$c$ 点时固体的颜色是红褐色
D.$d$ 点时溶液中有两种溶质
答案:15. B
解析:
【解析】
A. a点时固体质量仍在减少,说明${Fe_{2}O_{3}}$还在与稀盐酸反应,生成${FeCl_{3}}$,溶液中一定存在${Fe^{3+}}$,该选项正确;
B. b点时固体质量为0,说明${Fe_{2}O_{3}}$已完全反应,此时所加试剂可能是稀盐酸刚好反应完,也可能已经开始滴加${NaOH}$溶液(${NaOH}$先与过量稀盐酸反应,无沉淀生成),故所加试剂不一定是稀盐酸,该选项错误;
C. c点时,${NaOH}$与${FeCl_{3}}$反应生成红褐色的${Fe(OH)_{3}}$沉淀,固体颜色为红褐色,该选项正确;
D. d点时${NaOH}$过量,溶液中的溶质为反应生成的${NaCl}$和过量的${NaOH}$,共两种溶质,该选项正确。
【答案】
B
【知识点】
酸的化学性质;碱的化学性质;盐的化学性质
【点评】
本题结合图像考查酸、碱、盐的反应规律,需明确反应先后顺序,分析各阶段反应情况,对逻辑分析能力有一定要求。
【难度系数】
0.6
A. a点时固体质量仍在减少,说明${Fe_{2}O_{3}}$还在与稀盐酸反应,生成${FeCl_{3}}$,溶液中一定存在${Fe^{3+}}$,该选项正确;
B. b点时固体质量为0,说明${Fe_{2}O_{3}}$已完全反应,此时所加试剂可能是稀盐酸刚好反应完,也可能已经开始滴加${NaOH}$溶液(${NaOH}$先与过量稀盐酸反应,无沉淀生成),故所加试剂不一定是稀盐酸,该选项错误;
C. c点时,${NaOH}$与${FeCl_{3}}$反应生成红褐色的${Fe(OH)_{3}}$沉淀,固体颜色为红褐色,该选项正确;
D. d点时${NaOH}$过量,溶液中的溶质为反应生成的${NaCl}$和过量的${NaOH}$,共两种溶质,该选项正确。
【答案】
B
【知识点】
酸的化学性质;碱的化学性质;盐的化学性质
【点评】
本题结合图像考查酸、碱、盐的反应规律,需明确反应先后顺序,分析各阶段反应情况,对逻辑分析能力有一定要求。
【难度系数】
0.6
16. (15 分)某学习小组利用下列装置进行制取气体实验,请回答下列问题。
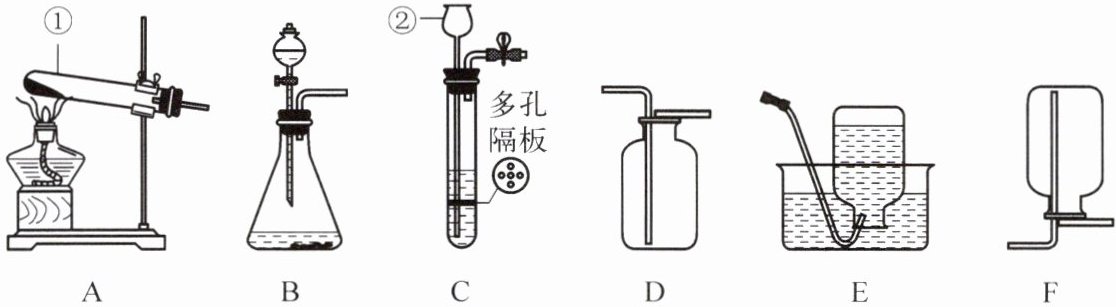
(1)仪器名称:①
(2)用双氧水和二氧化锰粉末制取 $O_2$,可选用装置
(3)实验室制取 $CO_2$ 的化学方程式为
(4)某学习小组利用如图 1 所示装置对氯酸钾制氧气进行探究学习。
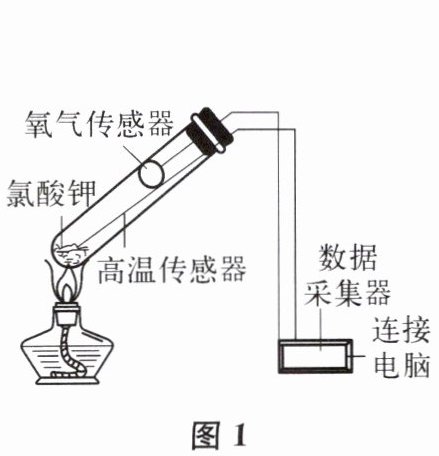

资料:Ⅰ. $KClO_3$ 的熔点约为 $356^{\circ}C$,$MnO_2$ 在加热条件下不分解。
Ⅱ. $KClO_3$ 分解时,传感器得到氧气浓度随温度的变化曲线如图 2 所示。
① 由图 1 分析,加热 $KClO_3$ 时试管口选择朝上的原因是
② 写出实验室用氯酸钾制取氧气的化学方程式:
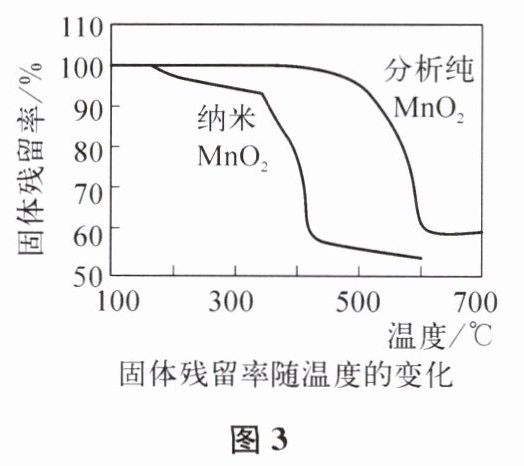
③ 分析图 3 可知,对 $KClO_3$ 分解催化效果更好的是

(1)仪器名称:①
试管
,②长颈漏斗
。(2)用双氧水和二氧化锰粉末制取 $O_2$,可选用装置
B
(填序号)和 E 组合,反应的化学方程式为$2H_2O_2\stackrel{MnO_2}{=}2H_2O + O_2\uparrow$
。选用 E 装置收集 $O_2$ 时检验是否收集满的方法是有气泡从集气瓶口向外均匀冒出,说明已收集满
。(3)实验室制取 $CO_2$ 的化学方程式为
$CaCO_3 + 2HCl = CaCl_2 + H_2O + CO_2\uparrow$
,选用装置 C 相对于 B 的优点是可控制反应的发生与停止
。(4)某学习小组利用如图 1 所示装置对氯酸钾制氧气进行探究学习。



资料:Ⅰ. $KClO_3$ 的熔点约为 $356^{\circ}C$,$MnO_2$ 在加热条件下不分解。
Ⅱ. $KClO_3$ 分解时,传感器得到氧气浓度随温度的变化曲线如图 2 所示。
① 由图 1 分析,加热 $KClO_3$ 时试管口选择朝上的原因是
防止氯酸钾熔化流出
。② 写出实验室用氯酸钾制取氧气的化学方程式:
$2KClO_3\stackrel{MnO_2}{\underset{\triangle}{=}}2KCl + 3O_2\uparrow$
。③ 分析图 3 可知,对 $KClO_3$ 分解催化效果更好的是
纳米
(填“纳米”或“分析纯”)$MnO_2$。答案:16. (1) ① 试管 ② 长颈漏斗 (2) B $2H_2O_2\stackrel{MnO_2}{=}2H_2O + O_2\uparrow$ 有气泡从集气瓶口向外均匀冒出,说明已收集满 (3) $CaCO_3 + 2HCl = CaCl_2 + H_2O + CO_2\uparrow$ 可控制反应的发生与停止 (4) ① 防止氯酸钾熔化流出 ② $2KClO_3\stackrel{MnO_2}{\underset{\triangle}{=}}2KCl + 3O_2\uparrow$ ③ 纳米